Detecção e identificação da malária
Introdução
A malária é uma doença global encontrada em regiões tropicais e subtropicais do mundo. Apesar das iniciativas internacionais destinadas a erradicar a doença, a malária ainda é responsável por mais de 600 mil mortes por ano – a maioria delas de crianças.
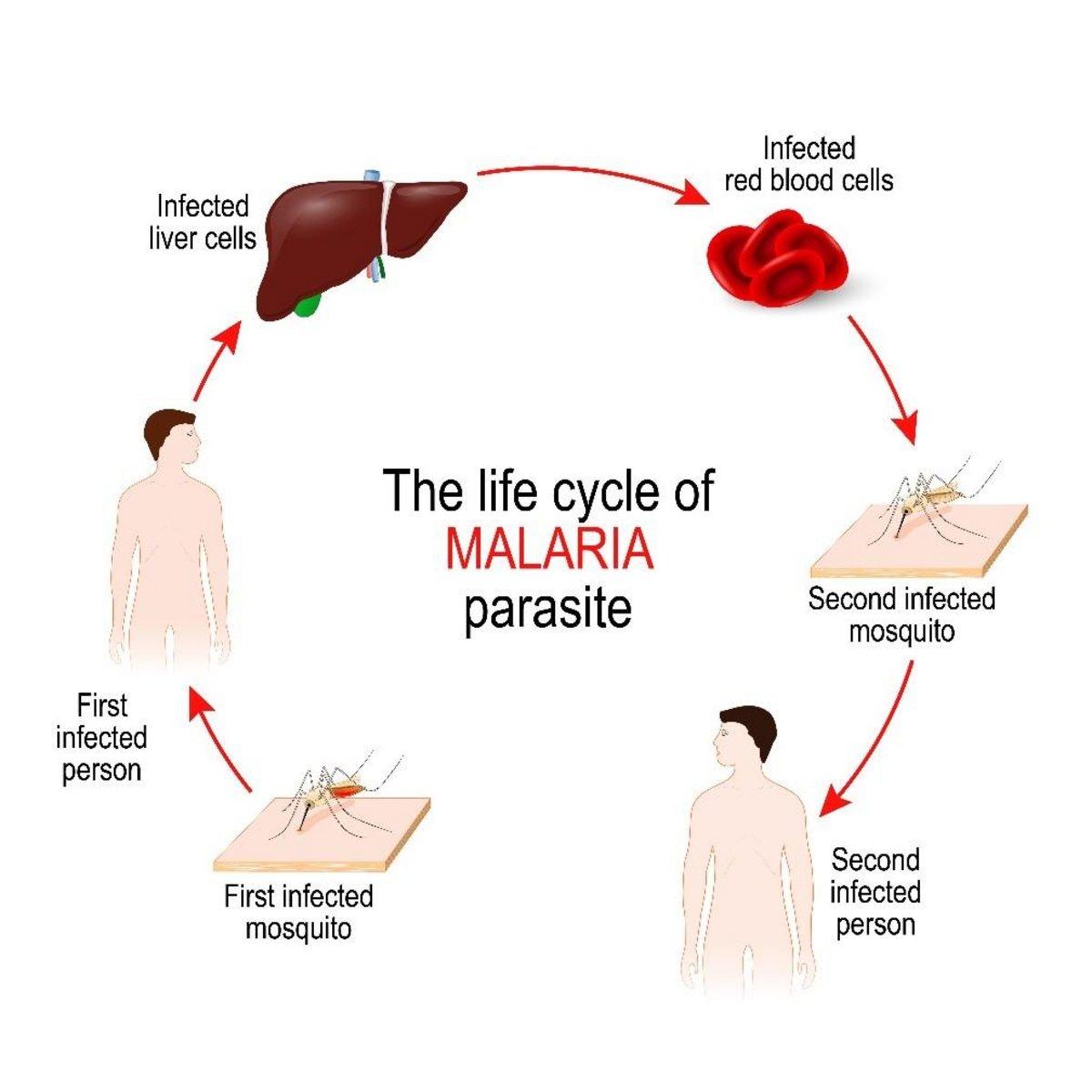
A malária é transmitida aos humanos pelo mosquito Anopheles. A picada do mosquito introduz o parasita na corrente sanguínea humana através de esporozoítos presentes na saliva. Os parasitas migram então para o fígado, onde amadurecem e se reproduzem. Esta fase é conhecida como fase exoeritrocítica. Os organismos se multiplicam no fígado, em hepatócitos infectados. Estes se diferenciam em milhares de merozoítos, que rompem a célula hospedeira, infiltrando-se na corrente sanguínea e infectando os glóbulos vermelhos. Esta próxima etapa é conhecida como fase eritrocítica do ciclo de vida. O parasita consegue sair do fígado sem ser detectado, pois se envolve na membrana das células hepáticas do hospedeiro infectado.
Sintomas
Os sinais e sintomas da malária são inespecíficos. A suspeita clínica de malária baseia-se principalmente na presença ou histórico recente de febre. Essa febre pode ser cíclica, correspondendo ao ciclo de vida do parasita; no entanto, não existe uma combinação de sinais ou sintomas que permita distinguir a malária de outras causas de febre de forma confiável.
Tipos de Malária
Existem cinco tipos conhecidos de parasitas da malária: Plasmodium falciparum, Plasmodium vivax, Plasmodium ovale, Plasmodium malariae e Plasmodium knowlesi. O mais grave é o P. falciparum e o menos comum é o P. knowlesi.
Plasmodium falciparum: encontrado principalmente na África, é o tipo mais comum de parasita da malária e responsável pela maioria das mortes por malária em todo o mundo, embora o tratamento cure a infecção.
Plasmodium Vivax: encontrado principalmente na Ásia e na América do Sul, esse parasita causa sintomas mais leves, mas pode permanecer no fígado por anos, o que pode resultar no reaparecimento dos sintomas se não for tratado adequadamente.
Plasmodium ovale: incomum e geralmente encontrado na África Ocidental.
Plasmodium malariae: esta doença é bastante rara e geralmente só é encontrada na África.
Plasmodium Knowlesi: esta espécie é muito rara e encontrada em partes do sudeste asiático.
Cada uma delas apresenta diferenças na aparência quando visualizadas em uma lâmina de sangue corada, o que auxilia na identificação. Veja a tabela abaixo:
Observação | P. Falciparum | P. Vivax | P. Malariae | P. Ovale |
|---|---|---|---|---|
| Tamanho (RBC) | Não ampliado | Ampliado | Não ampliado | Ampliado |
| Forma (RBC) | Redondo, às vezes crenado | Redondo ou oval | Redondo | Redondo ou oval, frequentemente com borda. |
| Cor (RBC) | Normal, mas pode escurecer ou apresentar uma borda roxa. | Normal a pálido | Normal | Normal |
| Pontilhado (RBC) | As manchas de Maurer aparecem como grandes manchas vermelhas, laços e fendas. | Os pontos de Schuffner aparecem como pequenos pontos vermelhos, numerosos. | Pontos de Ziemann, poucos pontos minúsculos, raramente detectados | Pontos de Schuffner (pontos de James). Numerosos pequenos pontos vermelhos. |
| Pigmento (RBC) | Preto ou castanho escuro | Visto como uma névoa de finos grânulos castanho-dourados dispersos pelo citoplasma. | Grânulos grossos pretos ou castanhos, dispersos | Intermediário entre P. Vivax e P. Malariae |
| Trofozoíto (parasita) | Pequenos, delicados, às vezes com dois pontos de cromatina, sendo comumente encontrados múltiplos anéis. | Relativamente grande, um ponto de cromatina, às vezes dois, frequentemente dois anéis em uma célula. | Compacto, um ponto de cromatina, único | Compacto, um ponto de cromatina, único |
| Esquizonte (parasita) | Tamanho médio | Grande | Pequeno | Médio |
| Gametócito (parasita) | em forma de crescente | Esférico | Semelhante ao P. Vivax, mas menor e menos frequente. | Semelhante ao P. Vivax, mas menor. |
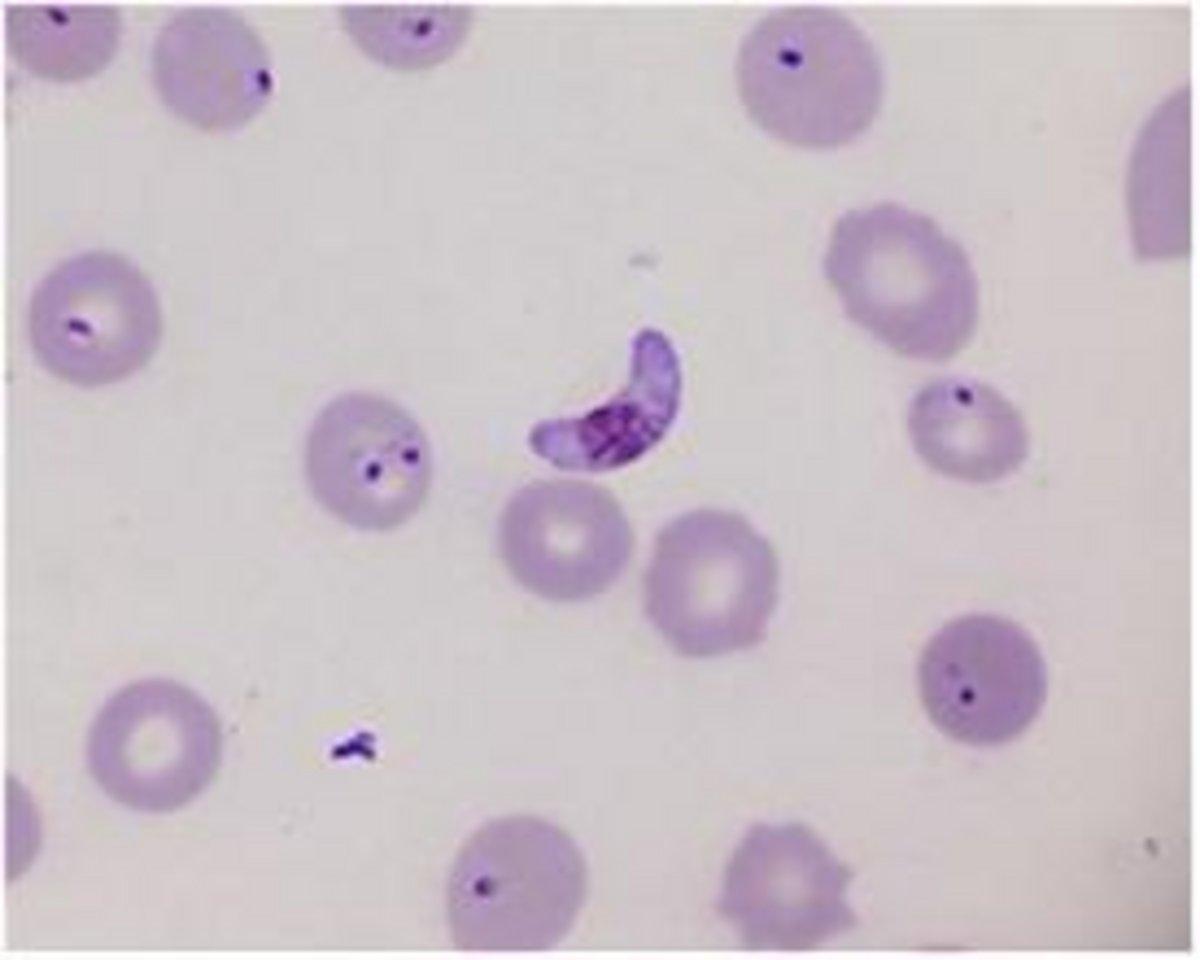
P. Falciparum- trofozoítos e gametócito em forma de crescente

P. Vivax- Gametócito (E) e trofozoíto (D)
Teste para Malária
O diagnóstico da malária é confirmado por exames de sangue, que podem ser microscópicos ou não microscópicos. Os exames microscópicos envolvem a coloração e a visualização direta do parasita ao microscópio. A visualização microscópica direta do parasita em esfregaços de sangue espesso e/ou fino tem sido o método aceito para o diagnóstico da malária na maioria dos contextos, desde o laboratório clínico até os levantamentos de campo, há mais de cem anos.
O exame cuidadoso de uma lâmina de sangue bem preparada e corada continua sendo o "padrão ouro" para o diagnóstico da malária.
Testes microscópicos
Lâminas espessas e finas de alta qualidade devem ser preparadas e examinadas em todos os casos suspeitos de malária, independentemente dos resultados dos testes rápidos de diagnóstico imunocromatográfico (TRD) ou de outros métodos de triagem para detecção de antígenos da malária.

Para detectar a presença de parasitas da malária, deve-se utilizar uma lâmina espessa, enquanto a lâmina fina serve para a identificação da espécie. É útil preparar quatro lâminas espessas e quatro finas, de forma que duas de cada possam ser coradas, deixando lâminas extras para envio a um centro de referência e para estudos adicionais, caso haja dificuldade diagnóstica.
As radiografias devem ser feitas o mais rápido possível para evitar a alteração morfológica dos parasitas que ocorre com o armazenamento de sangue anticoagulado com EDTA.
Após a coleta da amostra de sangue, o esfregaço é corado com corantes de Romanowski para examinar o aspecto intracelular dos glóbulos vermelhos.
Película espessa
A camada espessa de ágar com a densidade correta é aquela através da qual o papel de jornal é quase imperceptível. Ela é seca por 30 minutos e não fixada com metanol. Isso permite a hemólise dos glóbulos vermelhos, de modo que os leucócitos e quaisquer parasitas da malária presentes sejam os únicos elementos detectáveis. No entanto, devido à hemólise e à secagem lenta, a morfologia dos plasmódios pode ficar distorcida, dificultando a diferenciação das espécies. Portanto, as camadas espessas de ágar são utilizadas para detectar a infecção e estimar a concentração de parasitas.
Esfregaços sanguíneos espessos são geralmente corados pela técnica rápida de Field ou pela coloração de Giemsa para triagem de parasitas. A sensibilidade de um esfregaço sanguíneo espesso é de 5 a 10 parasitas/µl.
Película fina
Esfregaços finos permitem identificar as espécies de malária (incluindo o diagnóstico de infecções mistas), quantificar a parasitemia e avaliar a presença de esquizontes, gametócitos e pigmento malárico em neutrófilos e monócitos. Esfregaços sanguíneos finos corados com Giemsa ou Leishman são úteis para a especificação de parasitas e para a marcação de hemácias infectadas. O pH ideal da coloração é 7,2.
Kits de teste rápido (RTDs)
Os testes rápidos de diagnóstico (TRD) da malária complementam o diagnóstico da doença, fornecendo evidências da presença do parasita no sangue. Os TRD são utilizados em conjunto com a microscopia, principalmente em locais onde não há disponibilidade de profissionais com experiência em microscopia de alta qualidade.
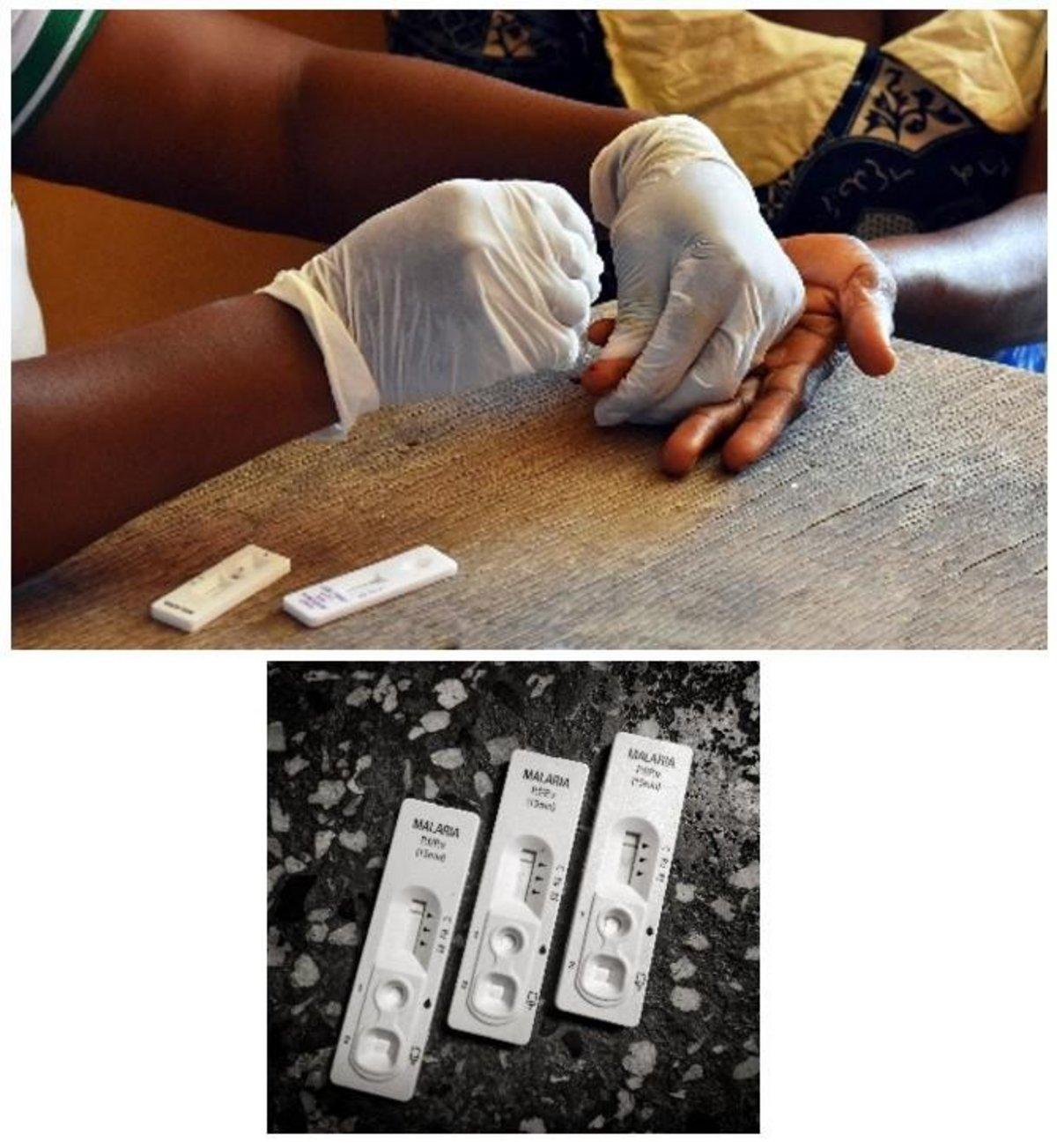
O teste funciona detectando antígenos específicos (proteínas) produzidos por parasitas da malária no sangue de indivíduos infectados. Trata-se de um teste imunocromatográfico de fluxo lateral para detecção de antígenos, que funciona capturando anticorpos marcados com corante para produzir uma banda visível em uma tira de nitrocelulose dentro de um cassete.
Nos testes rápidos de diagnóstico da malária (TRD), o anticorpo marcado com corante liga-se primeiro a um antígeno do parasita, e o complexo resultante é capturado na tira por uma faixa de anticorpo ligado, formando uma linha visível (linha T - linha de teste) na janela de resultados. Uma linha de controle (linha C - linha de controle) fornece informações sobre a integridade do conjugado anticorpo-corante, mas não confirma a capacidade de detectar o antígeno do parasita.
Alguns kits só conseguem detectar uma espécie (Plasmodium falciparum ou P. vivax), enquanto outros detectam várias espécies (P. falciparum, P. vivax, P. malariae e P. ovale).
Detecção por meio de hemograma completo
Como os parasitas da malária são encontrados no sangue periférico, sabe-se que eles interferem na contagem em analisadores de sangue completos. Os fabricantes podem, portanto, usar essas anormalidades para gerar alertas que avisem o operador sobre uma possível infecção por malária a partir de um hemograma completo.

HORIBA Medical desenvolveu um indicador de malária para diversos instrumentos, como o Microsemi CRP LC-667G e o ABX Pentra XL80, Pentra XLR, a partir de sinais encontrados nos canais de leucócitos.
Essa tecnologia foi aprimorada em uma série posterior de instrumentos, os modelos Yumizen H500 e Yumizen H550, que utilizam técnicas de aprendizado de máquina para criar um indicador de pontuação S para P. Falciparum, P. Vivax e dengue (este último é um vírus transmitido por mosquitos que produz sintomas semelhantes aos da malária).
Outros testes
Alguns laboratórios utilizam a análise quantitativa da camada leucocitária (QBC) em amostras positivas, porém este é um método dispendioso.
A PCR é outro método muito sensível e confiável para determinar a espécie de malária em infecções mistas. É utilizada principalmente em laboratórios de referência.
Conclusão
Em 2015, a Organização Mundial da Saúde (OMS) lançou uma Estratégia Técnica Global para a Malária 2016-2030 com o objetivo de reduzir a incidência e a mortalidade globais da malária em pelo menos 90% até 2030. As soluções técnicas incluem o controle do mosquito vetor, regimes aprimorados de tratamento e profilaxia, além de triagem e diagnóstico eficazes.
O acesso a testes laboratoriais e a disponibilidade de testes fáceis e rápidos desempenham um papel importante na conquista desse objetivo.
Agradecimentos
Este artigo foi reproduzido a partir do conteúdo dos boletins informativos QSP nº 24 e nº 25, que estão disponíveis aqui.
Autores: Kelly Duffy e Andrew Fisher da HORIBA UK Ltd.
Referências
https://www.ncbi.nlm.nih.gov/books/NBK555962/ (Bain, 2006; Bain et al, 2011)
https://www.who.int/teams/global-malaria-programme
Hematologia Essencial AV .Hoffbrand & JEPettit Moody AH, Chiodini PL.
Métodos para a detecção de parasitas sanguíneos. Clin Lab Haematol 2000;22:189-201