Technologia Double Hydrodynamic Sequential System (DHSS) to technologia opracowana przez HORIBA. Jej celem jest zapewnienie liniowego przepływu komórek poprzez metodę impedancji elektrycznej i pomiar optyczny, co pomaga w dokładnym różnicowaniu subpopulacji leukocytów (WBC) i płytek krwi. Podwójne ogniskowanie hydrodynamiczne to technika wykorzystywana do uzyskiwania dokładnych wyników z cytometru przepływowego. DHSS pomaga w specjalistycznym podejściu do analizy krwi.
DHSS_figure1_technology_image_HORIBA
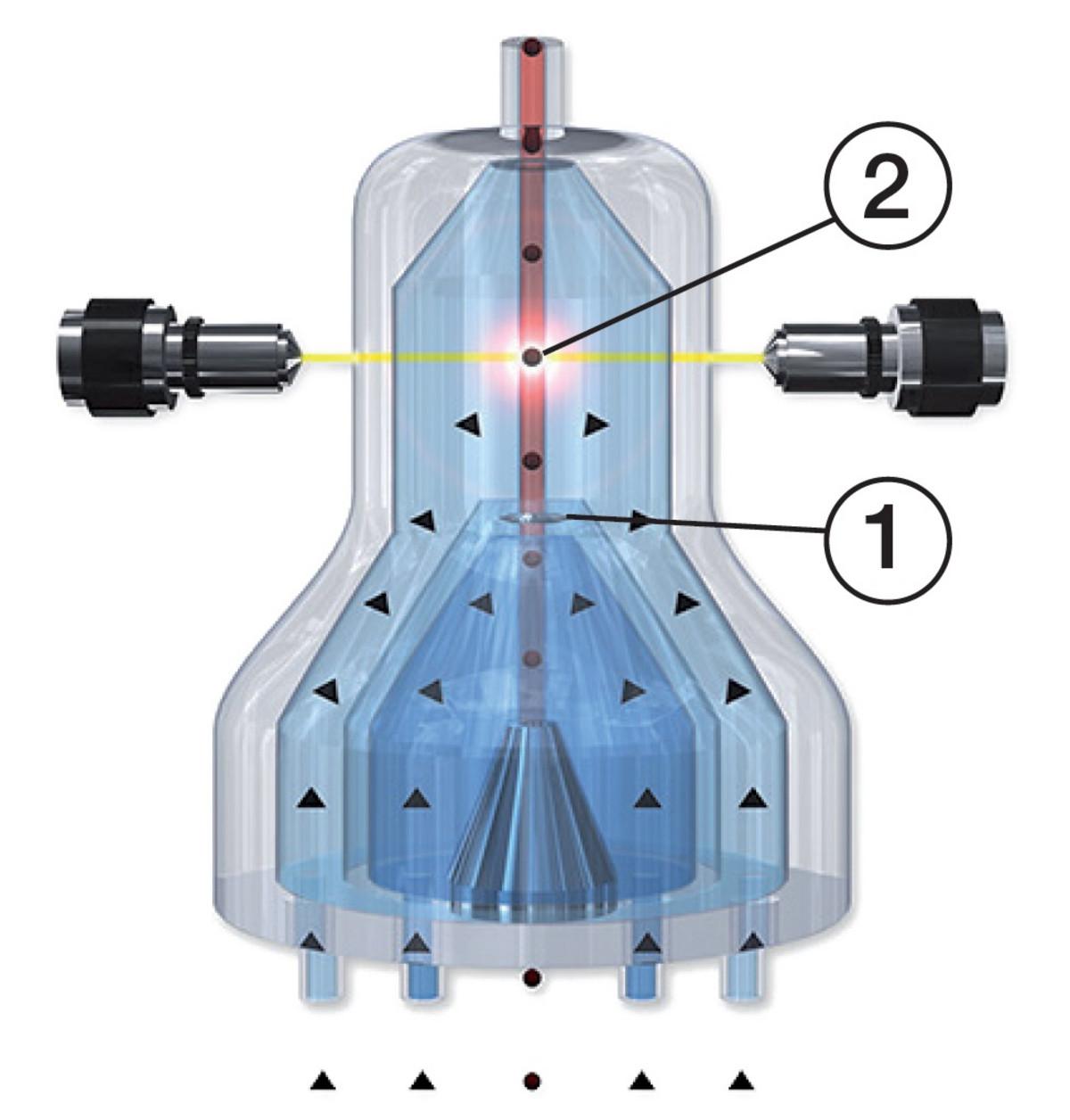
1. Komórki przechodzą przez otwór pojedynczo (① na rysunku 1), gdzie są liczone i mierzone za pomocą prądu elektrycznego (zmiany impedancji). Jest to pomiar rezystancji objętości komórki.
2. Następnie każda z nich przecina wiązkę światła, które dociera pod kątem 0° (➁ na rysunku 1), co pozwala określić złożoność komórek.
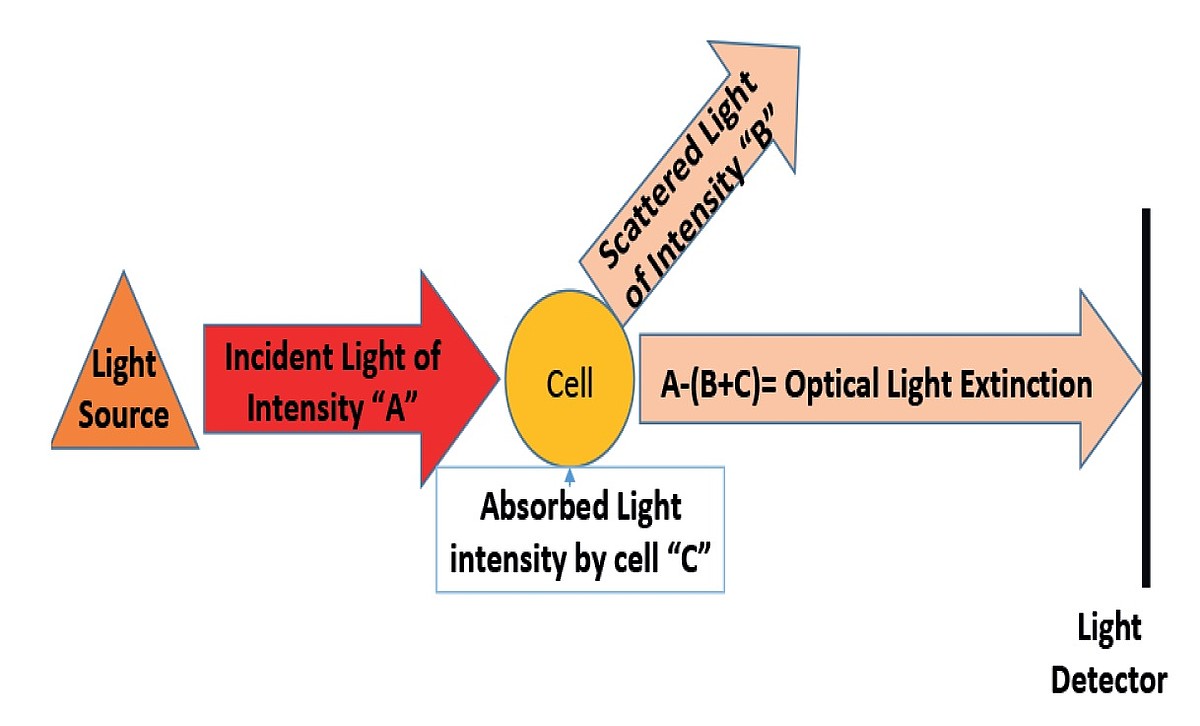
• Część światła jest pochłaniania przez zawartość komórki,
• Większa część jest odbijana przez struktury komórkowe (światło rozproszone),
• Reszta przechodzi przez komórkę lub wokół niej.
Analizatory HORIBA Medical wykorzystują połączenie pomiaru optycznego i impedancji elektrycznej do zliczania i analizy komórek przechodzących przez system elektrod z mikroaperturą. Impuls elektrody jest następnie wykorzystywany do zliczania komórek oraz pomiaru wielkości i rozmieszczenia leukocytów, erytrocytów i trombocytów.
DHSS_figure2_technology_image_HORIBA
Zasady pomiaru LMNE
Specjalny odczynnik HORIBA Nucediff lizuje erytrocyty i stabilizuje leukocyty (WBC) w ich naturalnej postaci. Następnie każda komórka jest mierzona pod kątem ekstynkcji optycznej (struktura wewnętrzna) i rezystywności (objętość), co pozwala na określenie całkowitej liczby komórek jądrzastych oraz różnicowanie limfocytów, monocytów, neutrofili, eozynofili, limfocytów atypowych, niedojrzałych populacji i erytroblastów.
cells_technology_image_HORIBA krwi
Zasada wykrywania LMNE opiera się na cytometrii przepływowej z wykorzystaniem podwójnego hydrodynamicznego układu sekwencyjnego (DHSS). Dla każdej komórki przechodzącej przez ten układ określane są dwie charakterystyki: objętość i wygaszenie światła optycznego.
Opis macierzy i komórek
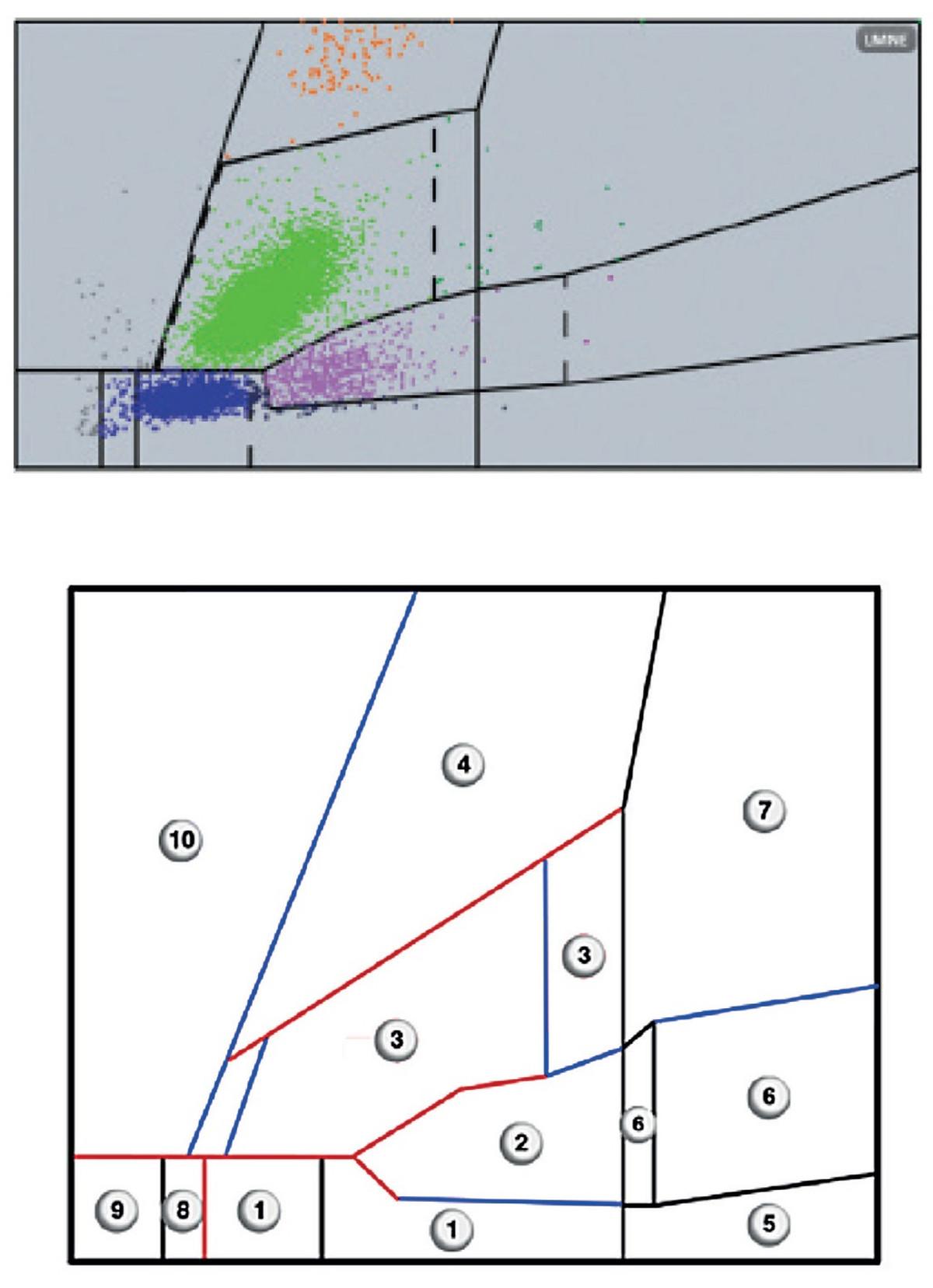
Rysunek 3: 1= Limfocyty 2= Monocyty 3= Neutrofile 4= Eozynofile 5= IML (Niedojrzałe komórki limfocytowe) 6= IMM (Niedojrzałe komórki monoocytowe) 7= IMG (Niedojrzałe komórki granulocytowe) 8= Erytroblasty lub agregaty płytek 9= Niski szum tła 10= Wysoki szum tła
Na podstawie pomiarów wygaszenia i oporności leukocytów tworzona jest macierz z objętościami komórek na osi X i wygaszaniem na osi Y. Badanie obrazu tła umożliwia wyraźne rozróżnienie subpopulacji leukocytów.
Progi populacji komórek (niektóre z nich są mobilne, a inne nieruchome) wyznaczają granice normalnej morfologii leukocytów. Zmiany w morfologii określonej populacji są oznaczone na macierzy przesunięciem w odpowiadającej jej populacji.
Stałe progi (rysunek 3) są zaznaczone na czarno, a progi ruchome na czerwono na powyższym rysunku. Niebieskie progi następują po czerwonych podczas dostosowywania macierzy. Macierz umożliwia obliczenie procentowej populacji leukocytów zgodnie z poniższym rysunkiem:
Erytroblasty (NRBC)
Erytroblasty to niedojrzałe krwinki czerwone z jądrem. Cytometr przepływowy wykrywa jądra komórek NRBC uwolnione po lizie ich błon przez Nucediff. Ze względu na niewielkie rozmiary i niską absorpcję, są one umieszczane w lewej części populacji limfocytów na matrycy (ramka nr 8 na rysunku 3). W tej strefie możemy również znaleźć agregaty płytek krwi. Urządzenie może je odróżnić od erytroblastów dzięki specyficznym algorytmom. W żadnym przypadku NRBC i agregaty płytek krwi nie są uwzględniane w liczbie leukocytów.
DHSS_figure4_technology_image_HORIBA
Morfologia komórkowa z DHSS:
W analizatorach HORIBA pomiar ekstynkcji jest wykonywany za pomocą źródła optycznego o niskiej koherencji. Źródło optyczne o niskiej koherencji charakteryzuje się różnymi składowymi widmowymi i przestrzennymi wiązki światła. Pomiar ten pozwala z jednej strony określić morfologię różnych organelli komórkowych, a z drugiej – charakterystykę wewnątrzcytoplazmatyczną. Wysoka apertura numeryczna wiązki światła umożliwia obserwację komórek.
Pomiar ten jest mniej wrażliwy na anizotropię komórki oraz jej położenie lub orientację w wiązce (rysunek 4) i dostarcza informacji zależnych od wewnętrznych cech komórki.
Źródło światła o niskiej spójności:
W przypadku światła polichromatycznego wykorzystującego wiązkę o niskiej spójności przestrzennej (wiązkę rozbieżną) pomiar jest mniej wrażliwy na położenie lub orientację komórki w wiązce.
Dlaczego światło spójne o niskim natężeniu, a nie światło laserowe?
Biorąc pod uwagę złożoność struktury i morfologii leukocytów, metoda identyfikacji i liczenia łącząca cytochemię i pomiar słabego światła koherentnego (oświetlenie o niskiej koherencji) okazuje się metodą lepiej różnicującą i bardziej niezawodną w porównaniu z metodami laserowymi.
DHSS_spectral light_laser_technology_image_HORIBA
| Laser | Lampa o niskim spójnym świetle | |
| Zalety | Duża moc w komorze przepływowej (90% mocy źródła światła). Nadaje się do fluorescencji. | Płaskość profilu intensywności wiązki. Bardzo niski poziom hałasu (wysoka częstotliwość). |
| Ograniczenia | Hałaśliwe światło, plamka, Trudne do precyzyjnego pomiaru objętości. Kształt światła gaussowskiego. | Niska wydajność (0,0004%). Zużycie energii elektrycznej, emisja ciepła. Nie nadaje się do fluorescencji. |
Pomiary optyczne wykonywane na analizatorach Yumizen pozwalają na uzyskanie dokładniejszych informacji na temat objętości, stosunku jądra do cytoplazmy i struktury wewnętrznej każdej komórki. Ta solidność jest szczególnie przydatna przy identyfikacji nieprawidłowości.
Analiza optycznego wygaszania płytek krwi
Podobnie jak w przypadku analizy WBC, płytki krwi zlicza się z wykorzystaniem sekwencyjnego systemu Double Hydrodynamic, gdy próbki są przetwarzane w trybie płytki optyczne. Tryb płytki optyczne odróżnia płytki krwi od populacji RBC na podstawie współczynnika refrakcji. Zasada pomiaru jest podobna do metody LMNE.
1. Po rozcieńczeniu roztwór jest przenoszony z komory na stół optyczny za pomocą odsysacza, a następnie analizowany w komorze pomiarowej. Rozcieńczony roztwór jest osłonięty podwójną osłoną hydrodynamiczną i przechodzi przez otwór kuwety przepływowej LMNE oraz okienko optyczne. Każda komórka jest mierzona zarówno pod względem rezystywności (objętości), jak i absorpcji (cytochemii).
2. Na podstawie tych pomiarów tworzona jest macierz, w której na osi X zaznaczone są objętości, a na osi Y ekstynkcja optyczna.
Rysunek 6: Reprezentacje macierzy PLTOx
PLT Ox:
Ten parametr odpowiada procentowej liczbie płytek krwi w stosunku do RBC zidentyfikowanych na matrycy, pomnożonej przez liczbę RBC zidentyfikowanych w komorze. Nie ma potrzeby kalibrowania tego parametru, ponieważ opiera się on na kalibracji RBC. Jednocześnie urządzenie wykonuje cykl RBC/PLT Low Value.
W jaki sposób podwójny hydrodynamiczny sekwencyjny system poprawia dokładność analizy hematologicznej?
Ogniskowanie hydrodynamiczne wykorzystuje przepływ w osłonie do kontrolowania częstotliwości próbkowania wewnątrz apertury i kierowania przepływu próbki wzdłuż jej centralnej osi. W tym przypadku podwójny sekwencyjny system hydrodynamiczny HORIBA zapobiega wpływowi efektów krawędziowych na wyniki i pomaga ustawić cząstki w tej samej orientacji.
Czym jest efekt krawędzi?
Obecność silniejszych gradientów elektrycznych w pobliżu krawędzi pola elektrycznego niż w jego centrum może wpływać na dokładność i zniekształcać wielkość impulsu elektrycznego, co skutkuje przeszacowaniem rozmiaru cząstki. Dzieje się tak, gdy cząstka przechodzi przez mikroaperturę w różnych pozycjach. Sytuację dodatkowo komplikuje orientacja cząstki w aperturze.
Zastosowanie DHSS pozwala uniknąć wielu potencjalnych problemów związanych z systemem apertury. Strumień próbki jest otoczony płynem osłonowym, gdy przechodzi przez centralną oś apertury. Przepływ laminarny pozwala centralnemu strumieniowi próbki na wystarczające zwężenie, aby oddzielić i ustawić komórki w pojedynczym rzędzie w celu przejścia przez strefę pomiaru. Zewnętrzny płyn osłonowy eliminuje recyrkulację komórek z powrotem do strefy pomiaru.
Bibliografia
1. Kachel V; Electrical Resistance Pulse sizing: Coulter sizing. Flow cytometry and Sorting. Second Edition, T. Willy & Sons, 1990; p 45-80.
2. Al Quddus N, moussa W.A and Bhattacharjee S., Motion of a spherical particle in a cylindrical channel using arbitrary Lanrangian-Eulerian method., J. Colloid and Interface Science, 2008; 317:620-630.
3. European patent EP 0 425 381, Apparatus for counting and determination of at least one leucocyte-subpopulation. Filing date: 25 october 1990; Lefevre D; Champseix H.; Champseix S.
4. BLOOD CELLS A practical Guide, Barbara J.Bain, Fourth edition (2006) Blackwell Publishing. Barbara J.Bain Professor of Diagnostic Haematology St Mary’s Hospital Campus of Imperial College Faculty of Medicine, London and Honorary Consultant Haematologist, St Mary’s Hospital London.
5. Optics of Biological Particles, series II: mathematics, Physics and Chemistry – Vol.238 NATO Science Series; Alfons Hoestra University of Amsterdam, The Netherlands. Valeri Maltsev Institute of Chemical Kinetics and Combustion, Novosibirsk, Russia. Gorden Videen Army Research Laboratory, Adelphi, MD, USA, University of Amsterdam, The Netherlands.
6. Lasers and Current Optical Techniques in Biology, Comprehensive series in photochemistry and photobiology- volume 4 RS.C , Giuseppe Palumbo Dipartemento di Biologia e Patologia Cellulare e Molecolare”L.Califano”, Università di Napoli “Federico II”, Napoli, Italia. Riccardo Pratesi Dipartimento di Fisica, Università di Firenze, Sesto Fiorentino (Fi), Italia.
7. Blood Cell Biology, Optics and Related Technologies, Readout HORIBA Technical Reports, English edition N°8, august 2004 . Philippe Nerin, Research Director Horiba Medical, PhD, Didier Lefèvre, R&D Department
8. Determination of volume, shape and refractive index of individual blood platelets; I.V. Kolesnikovaa,b, S.V. Potapovb, M. A. Yurkinb,c, A.G. Hoekstrac , V.P. Maltseva,b and K.A. Semyanovb, a Novosibirsk State University, Pirogova Str. 2, 630090, Novosibirsk, Russia b Institute of Chemical Kinetics and Combustion, Siberian Branch of the Russian Academy of Sciences, Institutskaya Str. 3, 630090, Novosibirsk, Russia c Faculty of Science, Section Computational Science, of the University of Amsterdam, Kruislaan 403, 1098 SJ, Amsterdam, The Netherlands.
9. UNDERSTANDING CONJUGATE PLANES AND KÖHLER ILLUMINATION Michael W. Davidson and Thomas J. Fellers; National High Magnetic Field Laboratory, The Florida State University, 1800 E. Paul Dirac Dr., Tallahassee, Florida 32306.
Analizator Hematologiczny
Analizator hematologiczny i OB
Masz pytania lub prośby? Skorzystaj z tego formularza, aby skontaktować się z naszymi specjalistami.