Autorzy: dr Rajesh Kumar Bhola, Shubham Rastogi,
Thomas Gibelin, Sebastien Raimbault, Christophe Fudaly (2024)
Płytki krwi lub trombocyty to małe, bezjądrowe, dyskoidalne fragmenty komórek o średnicy od 2 do 4 µm i objętości od 2 do 20 fL. Odgrywają one ważną rolę w pierwotnej hemostazie, zapaleniu lub wrodzonej odporności. Pochodzą z cytoplazmy megakariocytów (MK), jednych z największych (50-100 µm) i najrzadszych komórek w wąskim jądrze kostnym (0,01% komórek jądrzastych). Poprzez proces napędzany trombopoetyną (TPO), MK przechodzą 5-dniowe dojrzewanie, w którym stają się poliploidalne (128n) 1 i gromadzą białka oraz błonę. Poprzez proces napędzany cytoszkieletem rozszerzają się następnie do propłytek krwi, które są przekształcane w prepłytki. Podział prepłytek generuje płytki krwi, które przeżywają od 7 do 10 dni we krwi. 1 Średnia liczba płytek krwi wynosi od 150 do 410 x 10^9/l.
Analizator Hematologiczny Yumizen H2500 firmy HORIBA Evolutive Laboratory Organization (HELO 2.0) oferuje 8 różnych parametrów umożliwiających badanie populacji płytek krwi (rysunek 1).
| Parametry | Normalne zakresy | |||||||||||||||
| PLT | MPV | PLT-O | PCT* | PDW* | P-LCC* | P-LCR* | LPF* | |||||||||
| Bibliografia Granice | Dolne | Górna | Dolne | Górna | Dolne | Górna | Dolne | Górna | Dolne | Górna | Dolne | Górna | Dolne | Górna | Dolne | Górna |
| Męski | 160 | 362 | 7.4 | 11.5 | 148.1 | 399.9 | 0.1 | 0.3 | 11.4 | 19.1 | 44* | 140* | 18* | 50* | 1* | 12* |
| Kobieta | 172 | 411 | 7.6 | 11.8 | 152 | 374 | 0.16 | 0.37 | 11.8 | 19.6 | 44* | 140* | 18* | 50* | 1* | 12* |
| Bibliografia Dane 6 | 150 | 400 | 7.4 | 12 | 150 | 400 | 0.15 | 0.40 | 11 | 20 | * | * | * | * | * | * |
Rycina 1: Tabela zakresów norm dla każdego parametru związanego z płytkami krwi na podstawie badań HORIBA.
* Oznacza parametry wyłącznie badawcze (RUO). HORIBA, Raport o skuteczności klinicznej (CPR). DEV-CPR-2023-0009.
Zakresy te zostały ocenione na podstawie badania 240 próbek krwi pobranych z populacji francuskiej, analizowanych w dwóch powtórzeniach na jednym aparacie Yumizen H1500 i dwóch aparacie Yumizen H2500, zgodnie z normą CLSI C28-A3. 2 Pobieranie próbek od mężczyzn i kobiet przeprowadzono z użyciem antykoagulantu EDTA. Podane zakresy wartości prawidłowych różnią się w zależności od populacji badanych i/lub lokalizacji geograficznej. HORIBA zdecydowanie zaleca, aby każde laboratorium ustaliło własne zakresy wartości prawidłowych na podstawie lokalnej populacji.
Urządzenia HORIBA Yumizen H1500 i Yumizen H2500 mogą pomóc lekarzowi zidentyfikować pacjentów, u których parametry hematologiczne wykraczają poza ustalone zakresy referencyjne, poprzez zbieranie danych odzwierciedlających stan hematologiczny lub immunologiczny pacjenta w określonym momencie.
W połączeniu z innymi informacjami diagnostycznymi oraz oceną stanu pacjenta dokonaną przez lekarza prowadzącego, dane te przyczyniają się do postawienia diagnozy i zaplanowania leczenia klinicznego. Wynik poza zakresem referencyjnym dla badanej populacji może wskazywać na potencjalne znaczenie kliniczne. Dodatkowo, flagi ostrzegają operatora o nieprawidłowych populacjach komórek podczas procesu walidacji wyników.
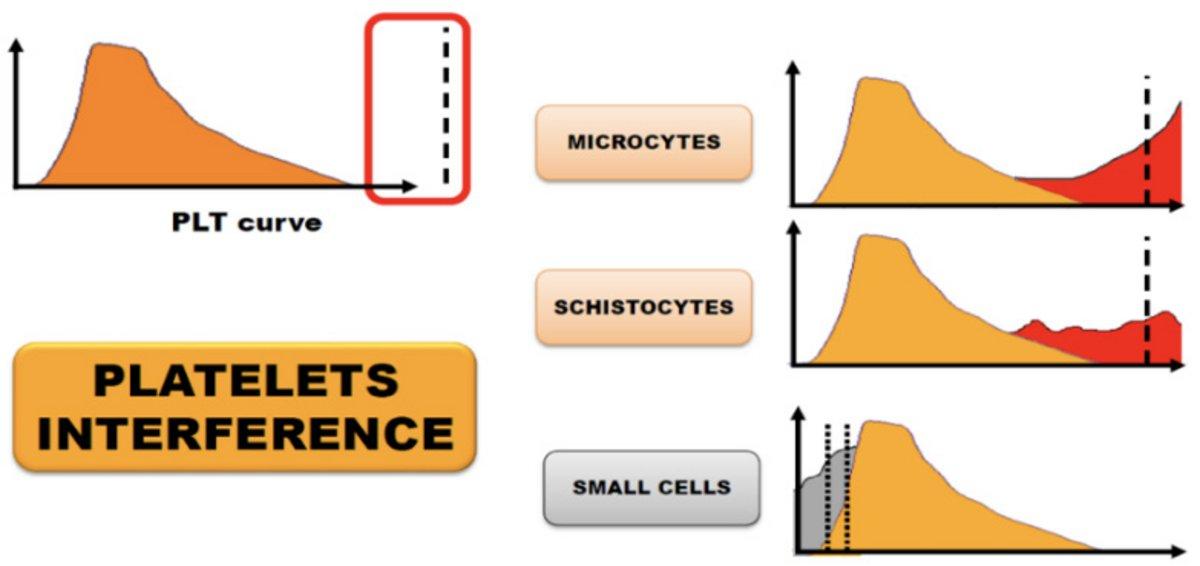
Rysunek 2: Zakłócenia RBC/PLT
Stężenie płytek krwi (PLT) to podstawowy parametr płytek krwi w morfologii krwi, który może wskazywać na trombocytopenię lub trombocytozę. MPV, czyli średnia objętość płytek krwi, jest wyprowadzana z krzywej rozkładu płytek krwi i mierzy średnią objętość populacji płytek krwi.
PLT-Ox, czyli analiza płytek krwi metodą optyczną, mierzy stężenie płytek krwi za pomocą impedancji i ekstynkcji optycznej, gdy technologia impedancyjna nie jest w stanie odróżnić dużych płytek krwi od interferencji ze strony mikrocytów lub pofragmentowanych erytrocytów. PCT, czyli analiza płytek krwi, mierzy całkowitą objętość płytek krwi i może wskazywać ilościowe anomalie płytek krwi. PDW, czyli analiza szerokości rozkładu płytek krwi, mierzy zmienność objętości płytek krwi i może wskazywać na heterogeniczność płytek krwi. P-LCR/P-LCC, czyli analiza stosunku/liczby dużych komórek płytek krwi, określa ilościowo każdą płytkę o objętości większej niż 12 flL, która może być dużą płytką krwi, agregatami płytek krwi lub mikrocytami. 3 LPF, czyli analiza frakcji dużych płytek krwi, mierzy populację dużych płytek krwi za pomocą technologii impedancji i ekstynkcji optycznej płytek krwi (PLT-Ox). Ekstynkcja optyczna umożliwia prawidłowe rozdzielenie krzywych RBC i PLT w przypadku występowania interferencji RBC/PLT spowodowanych obecnością olbrzymich płytek krwi, pofragmentowanych erytrocytów krwi, mikrocytów lub schistocytów (Rysunek 2).
Płytki krwi biorą udział w wielu różnych procesach biologicznych, więc nie jest zaskakujące, że krążące płytki krwi nie są sobie równe. Płytki krwi różnią się głównie gęstością i rozmiarem. Normalny zakres rozmiaru płytek krwi wynosi od 5 do 10 fL. Zatem frakcja dużych płytek krwi (LPF) odpowiada populacji płytek krwi większej niż 20 fL. Populacja ta składa się głównie z dużych młodych płytek krwi, zwanych również płytkami siateczkowatymi (RP) lub płytkami niedojrzałymi (IP). Młode płytki krwi/duże płytki krwi/RP są nowo uwolnione, większe i bardziej reaktywne. 4 Podobnie jak retikulocyty dla RBC, duże młode płytki krwi działają jako biomarkery w czasie rzeczywistym syntezy płytek krwi, znanej również jako trombopoeza. Duże młode płytki krwi zawierają nici RNA, które są wykorzystywane do syntezy białek. Jednakże nici te nie pochodzą z MK 4.
Przed wprowadzeniem metody LPF do badania liczebności populacji płytek krwi i ilościowego oznaczania dużych płytek krwi stosowano kilka parametrów, w tym MPV. MPV pozostaje stabilny u zdrowych osób, więc jego zmienność może wskazywać na proces chorobowy, na przykład w małopłytkowości immunologicznej, gdzie MPV wzrasta. 5 Zastosowano również PDW, P-LCC i P-LCR. Jednak te trzy parametry nie pozwalają na dokładną ilościową ocenę dużych płytek krwi. Oznaczenia P-LCC/P-LCR, oprócz dużych płytek krwi, mogą obejmować mikrocyty, schistocyty i agregaty płytkowe, co prowadzi do niedokładnego pomiaru liczby dużych płytek krwi.
Młode płytki krwi lub duże płytki krwi, zwane również płytkami siateczkowymi (RP), pozostają w krwiobiegu od 24 do 36 godzin 8. Po tym czasie zawartość i objętość RNA zmniejszają się. 4 Gęstość i rozmiar płytek krwi mogą wydawać się wskaźnikami wieku płytek krwi. Jednak według niektórych badań gęstość płytek krwi może lepiej odzwierciedlać wiek płytek krwi niż ich rozmiar 5,8. Zawartość RNA związana z gęstością płytek krwi jest zatem lepszym wskaźnikiem wieku. Niemniej jednak większość młodych płytek krwi lub RP to duże płytki krwi, a badanie wskazuje, że „większość płytek siateczkowych jest większa, przy czym około 90% jest ograniczonych do 50% subpopulacji dużych płytek krwi” 6. Zaobserwowano dodatnią korelację między procentem RP a wskaźnikami wielkości płytek krwi (MPV, P-LCR).
Frakcja dużych płytek krwi (LPF) składa się głównie z młodych płytek krwi/RP, ale także dużych płytek krwi, które nie są siateczkowate. Te płytki krwi są duże, ale niekoniecznie młode, ponieważ rozmiar nie jest dobrym markerem wieku płytek krwi. Ta populacja jest mniej aktywna pod względem syntezy białek. Jednak w przypadku RP, populacja ta prezentuje wyższy potencjał hemostatyczny ze względu na większy obszar kontaktu (15,8 fL) 5. W niektórych chorobach, takich jak choroby układu krążenia, wzrost populacji frakcji dużych płytek krwi, w tym płytek funkcjonalnie aktywnych, takich jak RP, wiąże się z gorszym rokowaniem. 7 Zatem badanie przesiewowe frakcji dużych płytek krwi może być przydatne w prognozowaniu i leczeniu różnych zaburzeń. Badanie przesiewowe LPF może być również przydatne w ocenie potrzeby transfuzji płytek krwi.
HORIBA Yumizen H2500 umożliwia badanie całej frakcji dużych płytek krwi. Nowy parametr frakcji dużych płytek krwi (LPF) dostarcza laboratoriom informacji, które umożliwiają diagnozę w ciągu kilku minut, bez konieczności wymiany sprzętu HORIBA Medical.
Duża liczba płytek krwi z wykorzystaniem parametru LPF zapewnia dokładne i wiarygodne wyniki dzięki połączeniu technologii impedancji i ekstynkcji optycznej. Sama impedancja jest dobra, ale niewystarczająca do zliczania płytek krwi ze względu na obecność resztek, mikrocytów lub agregatów płytkowych. Ekstynkcja optyczna jest funkcją objętości i indeksu optycznego. Indeks optyczny płytek krwi jest niższy niż indeks RBC, więc przy tej samej objętości ekstynkcja optyczna umożliwia rozróżnienie obu typów komórek, zapewniając większą dokładność niż sama impedancja.
Rysunek 3: HORIBA płytki optyczne metoda pomiaru z użyciem niespójnego źródła światła.
Tryb PLT-Ox (Platelet Optical Extinction) w analizatorze Yumizen umożliwia pomiar dwiema metodami: impedancją i ekstynkcją światła (absorbancją), które są łączone w celu uzyskania najbardziej wiarygodnego wyniku (rysunek 3).
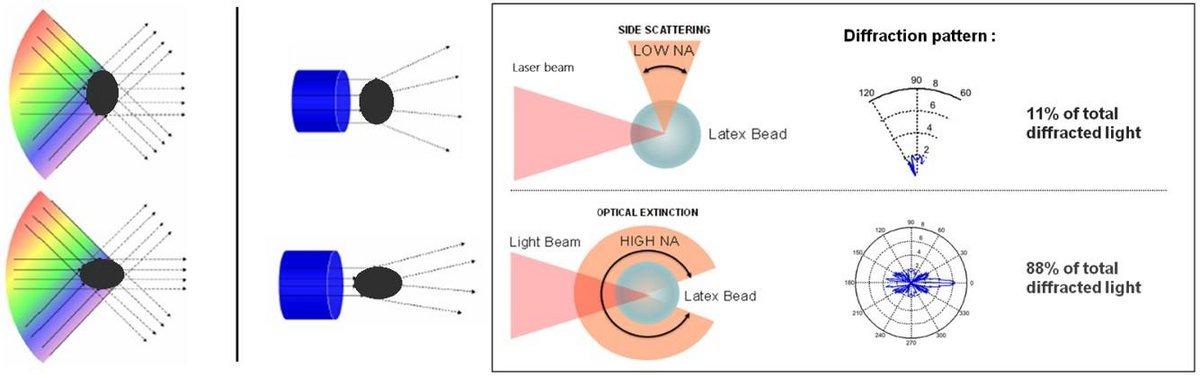
Technologia pomiaru ekstynkcji płytek krwi HORIBA wykorzystuje niespójne źródło światła (źródło rozszerzone). Wysoka apertura numeryczna wiązki światła umożliwia obserwację komórek pod różnymi kątami, ujawniając zarówno morfologię poszczególnych przedziałów komórkowych, jak i spektroskopowe charakterystyki wewnątrzcytoplazmatyczne.
W przeciwieństwie do monochromatycznego światła laserowego generującego idealnie równoległą wiązkę umożliwiającą obserwację komórki z jednego wymiaru, pomiary wykonane przy użyciu niespójnego źródła światła są mniej podatne na anizotropię komórki oraz jej położenie lub orientację w wiązce, dostarczając informacji o wewnętrznych cechach komórki (rysunek 4).
Rysunek 4: Rozpraszanie widmowe światła (po lewej) w porównaniu z rozpraszaniem generowanym laserowo (po prawej). Technologie laserowe i niekoherentne wiązki światła oraz odpowiadające im apertury numeryczne (NA) i wzory dyfrakcyjne.
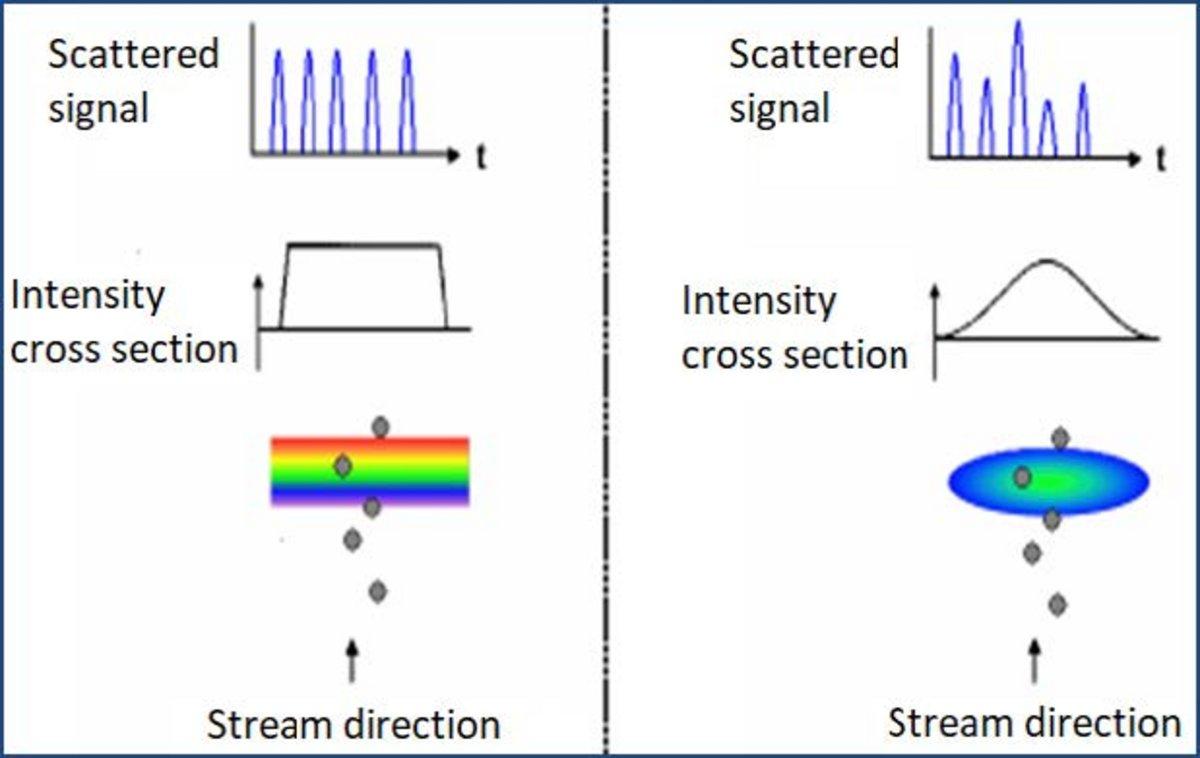
Rysunek 5: Rozpraszanie widmowe światła (po lewej) w porównaniu do rozpraszania generowanego laserowo (po prawej).
W przypadku spektralnego źródła światła, takiego jak laser monochromatyczny, sygnał związany z charakterystyką komórki jest silnie zależny od położenia i orientacji komórki w punkcie pomiarowym i musi być wyśrodkowany na osi. W przeciwnym razie odpowiedź świetlna może być zniekształcona i dawać różne wyniki, jak pokazano na rysunku 5. Przykład erytrocytów, które są idealnie anizotropowe, pokazuje, że wyniki byłyby całkowicie różne, gdyby nie były sferyczne.
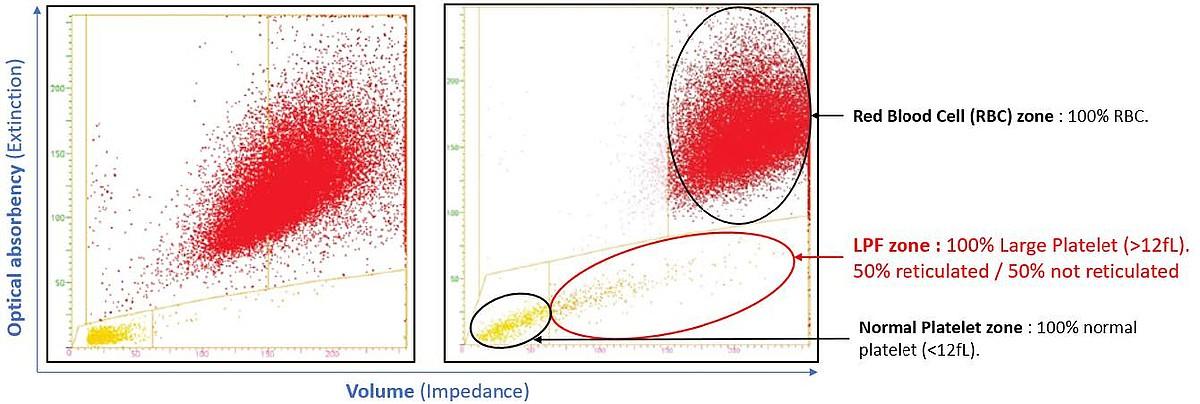
Tryb PLT-Ox różnicuje płytki krwi od populacji czerwonych krwinek (RBC) na podstawie współczynnika refrakcji. Każda komórka jest mierzona zarówno pod względem impedancji (objętości), jak i ekstynkcji optycznej. Na podstawie tych pomiarów tworzona jest matryca z objętościami na osi X i ekstynkcją optyczną na osi Y (rysunek 6). Parametr PLT-Ox odpowiada odsetkowi płytek krwi w stosunku do RBC zidentyfikowanych na matrycy, pomnożonemu przez liczbę RBC zidentyfikowanych w komorze pomiarowej. Nie ma potrzeby kalibracji tego parametru, ponieważ opiera się on na kalibracji RBC.
Rysunek 6: Wykresy rozrzutu płytek optycznych (PLT-O), niski poziom LPF (po lewej) w porównaniu z wysokim poziomem LPF (po prawej) z HORIBA Yumizen H2500.
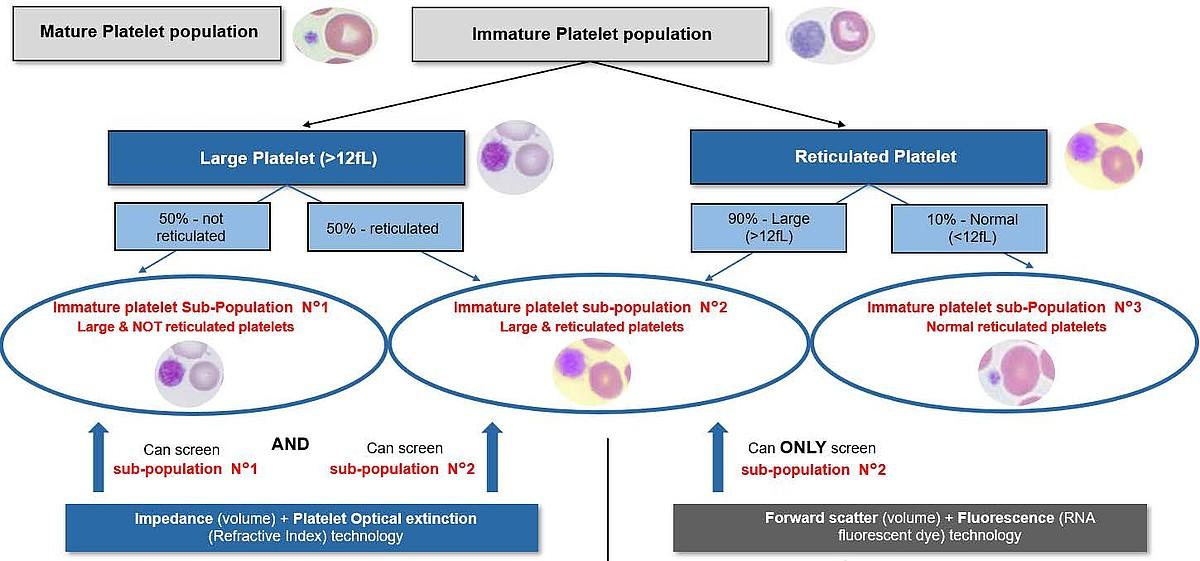
Parametr dużej frakcji płytek krwi związany z impedancją i technologią optycznego wygaszania płytek krwi umożliwia pełne pokrycie dużej populacji płytek krwi w porównaniu z technologią opartą na barwniku fluorescencyjnym RNA. Badanie 6 autorstwa V. Bodrova i wsp. ilustruje dużą populację płytek krwi i rozkład populacji siateczkowej (ryc. 7).
Rycina 7: Wizualna reprezentacja rozkładu dużych i siateczkowatych płytek krwi oraz technologia przesiewowa.
Ta wizualna reprezentacja wyraźnie pokazuje, że technologia HORIBA oferuje najlepsze pokrycie populacji dużych płytek krwi, co czyni ją odpowiednim narzędziem do badania dużych płytek krwi i wspomagania diagnozy.
Przeprowadzono porównawcze badanie kliniczne pomiędzy technologią HORIBA Large Platelet Fraction (bez fluorescencji) a technologią opartą na barwniku fluorescencyjnym RNA4. Łącznie 328 próbek krwi żylnej wybrano losowo, a po wykluczeniu wartości odstających przeanalizowano 272 próbki krwi żylnej. Kryteria doboru próbek to jedna grupa z MPV>11,5 fL, jedna grupa z MPV<11,5 fL, flaga schistocytów lub MCV <60 fL. Wszystkie próbki przetwarzano równolegle na obu analizatorach hematologicznych, w dwóch powtórzeniach i w ciągu 4 godzin od pobranie krwi. Przeprowadzono również ręczny przegląd preparatów zgodnie z wytycznymi CLSI H20-2A. Wszystkie wyniki zostały skorelowane, co wykazało dobrą korelację między tymi dwiema technologiami. Nowy parametr LPF może pomóc laboratoriom w podejmowaniu krytycznych decyzji i jest porównywalny z kryteriami wyboru próbek.
Obrót płytek krwi jest regulowany głównie przez TPO lub IL-1α w stanie zapalnym. TPO i IL-1α mogą promować syntezę i uwalnianie płytek krwi. Przy wysokim zapotrzebowaniu na płytki krwi obserwuje się wzrost liczby młodych, dużych płytek krwi lub płytek siateczkowatych. 5 Badania sugerują, że istnieje dodatnia korelacja między odsetkiem RP, rozmiarem płytek krwi i ich agregacją. 6 Przejście do wysokiej aktywności funkcjonalnej płytek krwi może wskazywać na zwiększone ryzyko zdarzeń zakrzepowych i jest również obserwowane w chorobach układu sercowo-naczyniowego. 5
Wysokie poziomy młodych płytek krwi/dużych płytek krwi/RP obserwuje się w rozsianym wykrzepianiu wewnątrznaczyniowym (DIC), zakrzepowej plamicy małopłytkowej (TTP), zespole hemolityczno-mocznicowym (HUS), immunologicznej plamicy małopłytkowej (ITP) oraz utracie krwi. Niski poziom RP obserwuje się w przypadku supresji zwężenia źrenicy, zespołów niewydolności zwężenia źrenicy, niedoborów żywieniowych lub mielosupresji polekowej. 7,8
W ostrym zespole sercowo-naczyniowym (ACS) ilościowe oznaczenie RP pomaga w ustaleniu rokowania (wysoki poziom RP wiąże się z gorszym rokowaniem) oraz w monitorowaniu leczenia przeciwpłytkowego, takiego jak inhibitory P2Y12.7 Badania wykazują, że w agregatach płytkowych występuje nadmierna ilość RP, ponieważ RP mają wyższy potencjał zakrzepowy, np. rekrutują trombinę.
W przypadku małopłytkowości, badanie przesiewowe młodych płytek krwi/RP może służyć do różnicowania rodzaju małopłytkowości. Wysoki poziom młodych płytek krwi/RP jest związany z małopłytkowością obwodową lub ostrą utratą krwi, natomiast niski poziom RP jest związany z małopłytkowością typu niewydolności szpiku kostnego (BMF).
W przypadku reaktywnej lub mieloproliferacyjnej trombocytozy, gdy obserwuje się wzrost liczby młodych płytek krwi/dużych płytek krwi/RP, istnieje większe ryzyko zakrzepicy. 4,8 W przypadku stanu przedrzucawkowego zwiększony poziom RP sugeruje aktywną trombopoezę mającą na celu kompensację zużycia płytek krwi. 4 Badanie przesiewowe poziomu młodych płytek krwi/dużych płytek krwi może być przydatne w przypadkach przeszczepu szpiku kostnego/komórek macierzystych w celu przewidywania regeneracji płytek krwi, a także może być wykorzystywane do podejmowania decyzji o odroczeniu profilaktycznej transfuzji płytek krwi u pacjentów poddawanych PBSC lub otrzymujących chemioterapię. 4
Badania przesiewowe dużej populacji płytek krwi mają znaczenie kliniczne. W związku z tym HORIBA, dzięki analizatorowi hematologicznemu Yumizen H2500 w wersji HELO 2.0, oferuje parametr frakcji dużych płytek krwi (LPF), co ułatwia diagnostykę i leczenie kliniczne.
Ten parametr opiera się na dokładnej i niezawodnej technologii, łączącej impedancję i ekstynkcję optyczną płytek krwi. Technologia ta oferuje najlepsze pokrycie i przesiew populacji młodych dużych płytek krwi dostępnych na rynku.
(1) Machlus, KR; Italiano, JE Niesamowita podróż: od rozwoju megakariocytów do formowania płytek krwi. J. Cell Biol.2013, 201 (6), 785–796. doi.org/10.1083/jcb.201304054.
(2) Sułtan Claude. Aide-mémoire d'hématologie / C. Sultan, M. Gouault-Heilmann, M. Imbert... ; z współpracą C. André, B. Genetet, L. Intrator... [i in.], [3e édition].; Aide-mémoire; Flammarion Nauki Medycyne: Paryż, 1987.
(3) Dharap, P. PLATELET INDEXS: Proste i skuteczne narzędzie do monitorowania chorób. Biuletyn2021
(4) Buttarello, M.; Mezzapelle, G.; Freguglia, F.; Plebani, M. Retikulowane płytki krwi i frakcja niedojrzałych płytek: zastosowania kliniczne i ograniczenia metody. Int. J. Lab. Hematol.2020,42 (4), 363–370. doi.org/10.1111/ijlh.13177.
(5) Handtke, S.; Thiele, T. Duże i małe płytki krwi – (kiedy) się różnią? J. Thromb. Haemost. JTH2020,18 (6), 1256–1267. doi.org/10.1111/jth.14788.
(6) Bodrova, V. V.; Shustova, O. N.; Chaspekowa, S. G.; Mazurow, A. V. Kreskówkowe formy płytek krwi, indeksy rozmiaru i aktywność funkcjonalna. Interakcje u zdrowych wolontariuszy. Płytki2021, 1–6. doi.org/10.1080/09537104.2021.1922659.
(7) Ali, S. A.; Shaikh, M. S. Kliniczne zastosowanie frakcji niedojrzałych płytek krwi – zaawansowany parametr w hematologii laboratoryjnej. J. Coll. Physicians Surg.--Pak. JCPSP2016,26 (9), 798–799. doi.org/2441.
(8) Płytki duże i małe — (Kiedy) się różnią? Stefan Handtke, Thomas Thiele. Artykuł przeglądowy, zaakceptowany: 25 lutego 2020, DOI: 10.1111/jth.14788
Analizator Hematologiczny
Masz pytania lub prośby? Skorzystaj z tego formularza, aby skontaktować się z naszymi specjalistami.