Malaria Detection and Identification
Wstęp
Malaria to choroba o zasięgu globalnym, występująca w tropikalnych i subtropikalnych regionach świata. Pomimo międzynarodowych inicjatyw mających na celu jej wyeliminowanie, malaria nadal jest przyczyną ponad 600 000 zgonów rocznie – głównie dzieci.
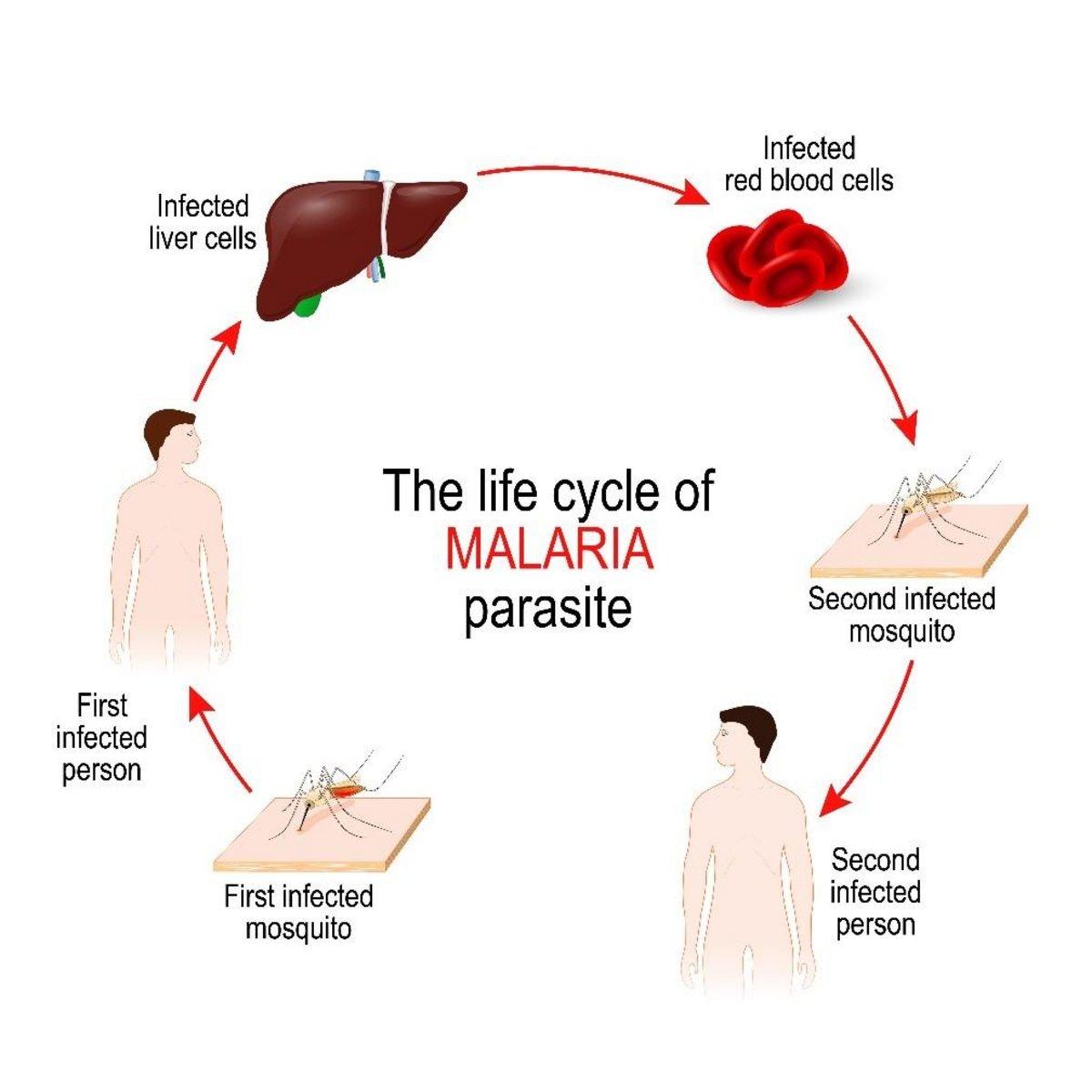
Malaria jest przenoszona na ludzi przez komara z rodzaju Anopheles. Ukąszenie komara wprowadza pasożyta do krwiobiegu człowieka za pośrednictwem sporozoitów w ślinie. Pasożyty migrują następnie do wątroby, gdzie dojrzewają i rozmnażają się. Faza ta znana jest jako faza egzoerytrocytarna. Organizmy namnażają się w wątrobie w zakażonych hepatocytach. Różnicują się w tysiące merozoitów, które rozrywają komórkę gospodarza, przenikając do krwi i infekując czerwone krwinki. Ten kolejny etap cyklu życiowego znany jest jako faza erytrocytarna. Pasożyt może opuścić wątrobę niezauważony, ponieważ otula się błoną komórkową wątroby zakażonego gospodarza.
Objawy
Objawy malarii są niespecyficzne. Podejrzenie malarii klinicznie stawia się przede wszystkim na podstawie aktualnej lub niedawnej gorączki w wywiadzie. Gorączka może mieć charakter cykliczny, zgodnie z cyklem życiowym pasożyta, jednak nie ma kombinacji objawów, która wiarygodnie odróżniałaby malarię od innych przyczyn gorączki.
Rodzaje malarii
Znanych jest pięć rodzajów pasożyta wywołującego malarię: Plasmodium falciparum, Plasmodium Vivax, Plasmodium ovale, Plasmodium malariae i Plasmodium Knowlesi. Najgroźniejszym jest P. falciparum, a najrzadszym P. Knowlesi.
Plasmodium falciparum: występuje głównie w Afryce, jest najczęstszym rodzajem pasożyta malarii i odpowiada za większość zgonów z powodu malarii na świecie, choć istnieje skuteczne leczenie infekcji
Plasmodium Vivax: pasożyt ten występuje głównie w Azji i Ameryce Południowej. Powoduje łagodniejsze objawy, jednak może pozostawać w wątrobie przez wiele lat, co może doprowadzić do nawrotu objawów, jeśli choroba nie jest odpowiednio leczona.
Plasmodium Ovale: rzadki, zwykle występujący w Afryce Zachodniej.
Plasmodium Malariae: dość rzadki i zazwyczaj występuje jedynie w Afryce.
Plasmodium Knowlesi: bardzo rzadki gatunek, występujący w południowo-wschodniej Azji.
Każdy z nich różni się wyglądem na barwionym rozmazie krwi, co ułatwia identyfikację, patrz poniższa tabela:
Obserwacja | P. Falciparum | P. Vivax | P. Malariae | P. Ovale |
|---|---|---|---|---|
| Rozmiar (RBC) | Nie powiększone | Powiększone | Nie powiększone | Powiększone |
| Kształt (RBC) | Okrągłe, czasami z wypustkami | Okrągłe lub owalne | Okrągłe | Okrągłe lub owalne, często z "postrzępionym" brzegiem |
| Kolor (RBC) | Normalny, ale może ciemnieć lub mieć fioletową obwódkę | Normalny do bladego | Normalne | Normalne |
| Nakrapianie (RBC) | Plamki Maurera pojawiają się jako duże czerwone plamki, pętle i szczeliny | Kropki Schuffnera pojawiają się jako liczne, małe czerwone kropki | Kropki Ziemanna, kilka maleńkich kropek, rzadko wykrywane | Kropki Schuffnera (kropki Jamesa). Liczne małe czerwone kropki |
| Wybarwienie (RBC) | Czarne lub ciemnobrązowe | Widziane jako mgła drobnych, złocistobrązowych ziarenek rozsianych po cytoplazmie | Rozproszone, czarne lub brązowe grube ziarna | Pośrednie między P. Vivax a P. Malariae |
| Trofozoit (pasożyt) | Małe, delikatne, czasami dwie kropki chromatyny, często spotykane są liczne pierścienie | Stosunkowo duży, jeden punkt chromatyny, czasami dwa, często dwa pierścienie w jednej komórce | Kompaktowy, pojedyncza kropka chromatyny | Kompaktowy, pojedyncza kropka chromatyny |
| Schizont (pasożyt) | Średni rozmiar | Duży | Mały | Średni |
| Gametocyt (pasożyt) | Półksiężyc | Kulisty | Podobne do P. Vivax, ale mniejsze i rzadsze | Jak P. Vivax, ale mniejsze |
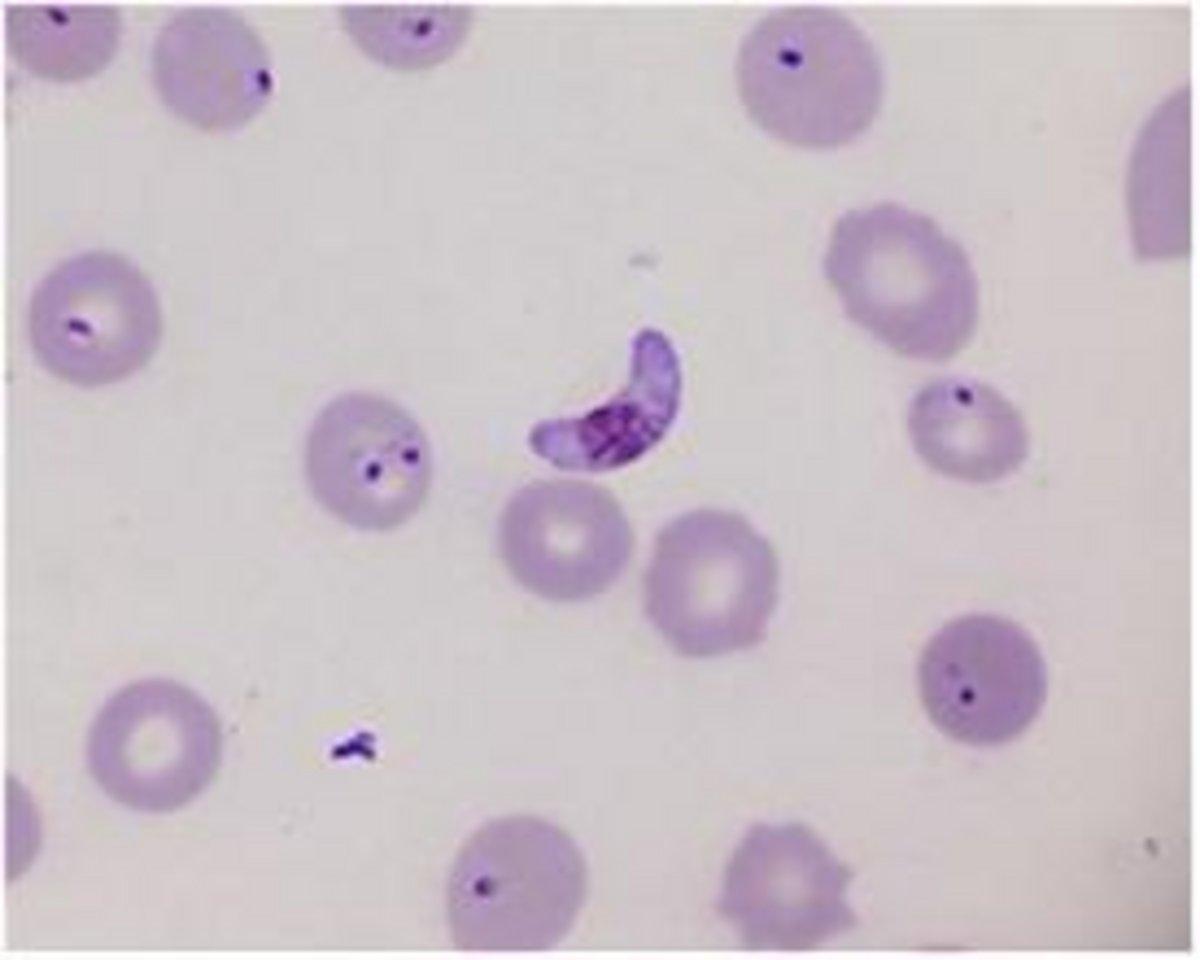
P. Falciparum- trofozoity i półksiężycowate gametocyty

P. Vivax- Gametocyt (L) i trofozoit (R)
Testowanie na malarię
Diagnozę malarii potwierdzają badania krwi, które są mikroskopowe lub niemikroskopowe. Badania mikroskopowe obejmują barwienie i bezpośrednią wizualizację pasożyta pod mikroskopem. Bezpośrednia mikroskopowa wizualizacja pasożyta na grubych i/lub cienkich rozmazach krwi jest akceptowaną metodą diagnozowania malarii w większości przypadków, od laboratoriów klinicznych po badania terenowe, od ponad stu lat.
Obecnie „złotym standardem” w diagnostyce malarii pozostaje dokładna analiza dobrze przygotowanego i dobrze zabarwionego rozmazu krwi.
Badania mikroskopowe
Przy każdym podejrzeniu malarii należy wykonać i zbadać wysokiej jakości, grube i cienkie rozmazy, niezależnie od wyników szybkich immunochromatograficznych testów diagnostycznych (RDT) lub innych metod przesiewowych służących do wykrywania antygenu malarii.

Do wykrywania obecności pasożytów malarii należy stosować gruby rozmaz, a cienki do identyfikacji gatunków. Warto przygotować cztery grube i cztery cienkie rozmazy, aby można było wybarwić po dwa z każdego rodzaju, pozostawiając zapasowe rozmazy do wysłania do ośrodka referencyjnego i dalszych badań w przypadku trudności diagnostycznych.
Rozmazy należy wykonać możliwie jak najszybciej, aby uniknąć zmian morfologicznych pasożytów, które mogą wystąpić podczas przechowywania krwi z dodatkiem EDTA jako środka przeciwzakrzepowego.
Po pobraniu próbki krwi, rozmaz jest barwiony barwnikiem Romanowskiego w celu zbadania wyglądu wewnątrzkomórkowego czerwonych krwinek.
Gruba warstwa
Gruba warstwa o prawidłowej gęstości to taka, przez którą ledwo widać papier gazetowy. Jest ona suszona przez 30 minut i nie jest utrwalana metanolem. Pozwala to na hemolizę czerwonych krwinek, a jedynymi wykrywalnymi elementami będą leukocyty i ewentualne pasożyty malarii. Jednak z powodu hemolizy i powolnego suszenia morfologia malarii może ulec zniekształceniu, co utrudnia różnicowanie gatunków. Grube warstwy są zatem wykorzystywane do wykrywania infekcji i szacowania stężenia pasożytów.
Grube rozmazy krwi są zazwyczaj barwione szybką techniką Fielda lub metodą Giemsy w celu wykrycia pasożytów. Czułość grubego rozmazu krwi wynosi 5-10 pasożytów/µl.
Cienka warstwa
Cienkie rozmazy pozwalają na identyfikację gatunków malarii (w tym diagnostykę zakażeń mieszanych), ilościową ocenę parazytemii oraz ocenę obecności schizontów, gametocytów i barwnika malarii w neutrofilach i monocytach. Cienkie rozmazy krwi barwione metodą Giemsy lub Leishmana są przydatne do identyfikacji pasożytów i punktowego oznaczania zakażonych krwinek czerwonych. Optymalne pH barwienia wynosi 7,2.
Zestawy do szybkiego testowania (RTD)
Szybkie testy diagnostyczne malarii (RDT) uzupełniają diagnostykę malarii, dostarczając dowodów na obecność pasożytów malarii we krwi. Testy RDT są stosowane jako uzupełnienie mikroskopii, szczególnie w przypadku braku doświadczenia w zakresie mikroskopii wysokiej jakości.
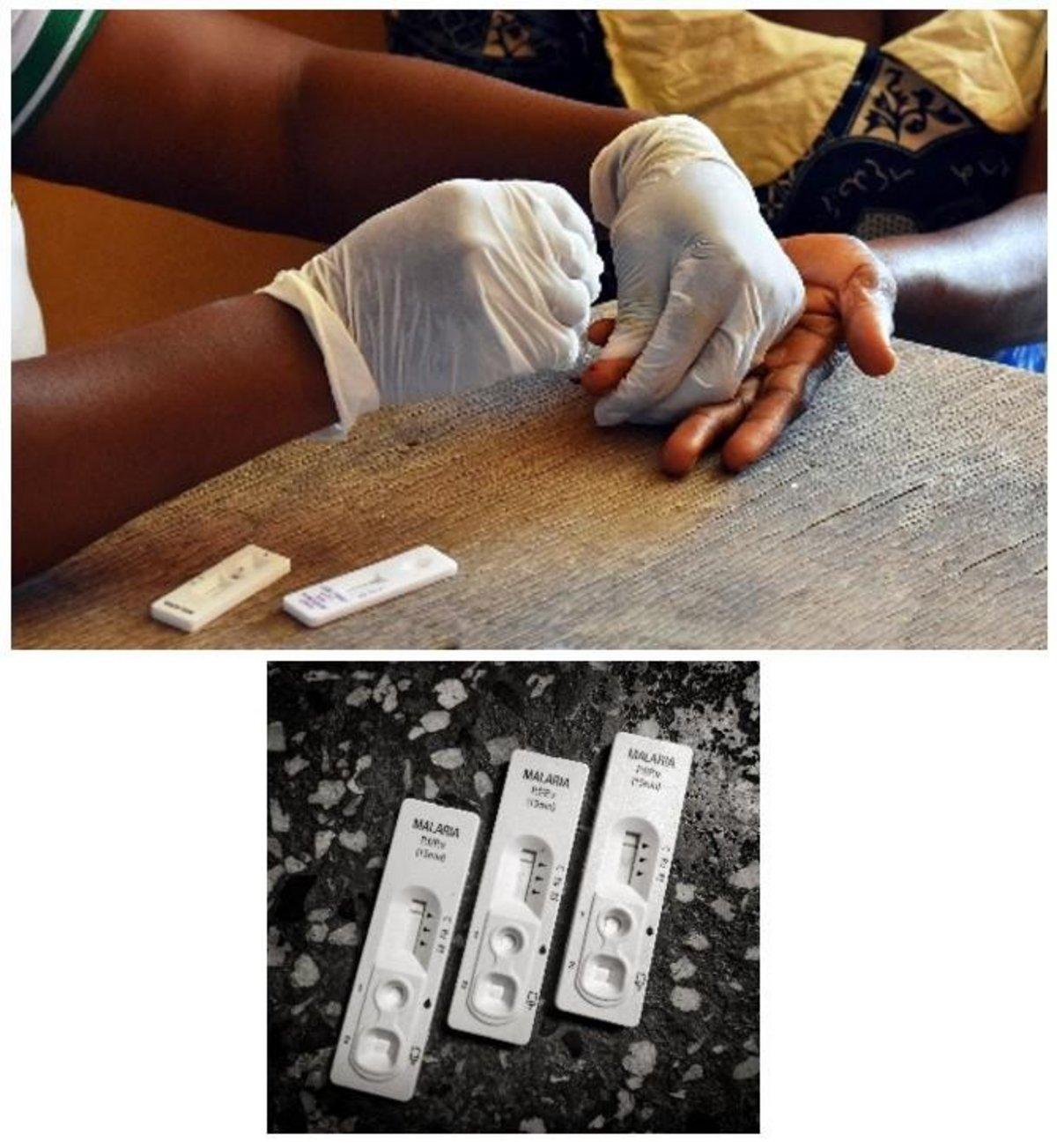
Test działa poprzez wykrywanie specyficznych antygenów (białek) wytwarzanych przez pasożyty malarii we krwi osób zakażonych. Jest to immunochromatograficzny test detekcji antygenów z przepływem bocznym, który działa poprzez wychwytywanie znakowanych barwnikiem przeciwciał w celu utworzenia widocznego pasma na pasku nitrocelulozy w obudowie kasety.
W przypadku testów RDT przeciwko malarii, przeciwciało znakowane barwnikiem najpierw wiąże się z antygenem pasożyta, a powstały kompleks jest wychwytywany na pasku przez pasmo związanego przeciwciała, tworząc widoczną linię (T – linia testowa) w okienku wyników. Linia kontrolna (C – linia kontrolna) dostarcza informacji o integralności koniugatu przeciwciało-barwnik, ale nie potwierdza zdolności do wykrywania antygenu pasożyta.
Niektóre zestawy umożliwiają wykrycie tylko jednego gatunku (Plasmodium falciparum lub P. vivax), inne zaś wykrywają wiele gatunków (P. falciparum, P. vivax, P. malariae i P. ovale).
Wykrywanie poprzez pełną morfologię krwi
Ponieważ pasożyty wywołujące malarię znajdują się we krwi obwodowej, wiadomo, że zakłócają one liczenie komórek krwi w analizatorach. Producenci mogą zatem wykorzystać te nieprawidłowości do generowania flag ostrzegających operatora o potencjalnym zakażeniu malarią na podstawie pełnej morfologii krwi.

HORIBA Medical opracowała flagę malarii dla kilku instrumentów, Microsemi CRP LC-667G i ABX Pentra XL80, Pentra XLR, na podstawie sygnałów znalezionych w kanałach WBC.
Technologia ta została rozwinięta w późniejszej serii instrumentów, Yumizen H500 i Yumizen H550, wykorzystując techniki uczenia maszynowego do utworzenia flagi S-score dla P. Falciparum, P. Vivax i Dengue (ten ostatni to wirus przenoszony przez komary, który wywołuje objawy podobne do malarii).
Inne testy
Niektóre laboratoria stosują ilościową analizę kożuszka leukocytarnego (QBC) w przypadku próbek dodatnich, jest to jednak droga metoda.
PCR to kolejna metoda, która jest bardzo czuła i wiarygodna w określaniu gatunku malarii w przypadku zakażenia mieszanego. Jest ona stosowana głównie w laboratoriach referencyjnych.
Wniosek
Światowa Organizacja Zdrowia (WHO) w 2015 r. opublikowała Globalną Strategię Techniczną dotyczącą malarii na lata 2016–2030, której celem jest zmniejszenie globalnych wskaźników zachorowań i zgonów z powodu malarii o co najmniej 90% do 2030 r. Rozwiązania techniczne obejmują kontrolę komarów będących wektorami choroby, ulepszone metody leczenia i profilaktyki, a także skuteczne badania przesiewowe i diagnostykę.
Dostęp do badań laboratoryjnych oraz możliwość łatwego i szybkiego przeprowadzania testów odgrywają ważną rolę w osiągnięciu tego celu.
Podziękowanie
Niniejszy artykuł jest przedrukowaną treścią Biuletynów QSP nr 24 i 25, które są dostępne tutaj.
Autorzy: Kelly Duffy i Andrew Fisher z HORIBA UK Ltd.
Bibliografia
https://www.ncbi.nlm.nih.gov/books/NBK555962/ (Bain, 2006; Bain i in., 2011)
https://www.who.int/teams/global-malaria-programme
Essential Haematology A.V. Hoffbrand & J.E. Pettit Moody AH, Chiodini PL.
Methods for the detection of blood parasites. Clin Lab Haematol 2000;22:189-201