Nasze ciała są stale narażone na patogeny obecne w środowisku, w tym wirusy, bakterie, pasożyty i grzyby. Odpowiedź immunologiczna odpowiada za obronę przed nimi poprzez szeroki zakres mechanizmów. Jest ona pośredniczona przez białe krwinki (WBC), zwane również leukocytami, do których należą neutrofile, eozynofile (acidofile), bazofile, limfocyty i monocyty. Odporność wrodzona i nabyta współpracują ze sobą, aby nas chronić (1).
WBC fagocytujące (w szczególności neutrofile) są częścią wrodzonej gałęzi układu odpornościowego, wraz z makrofagami tkankowymi, które pełnią szereg różnych funkcji, takich jak inicjowanie odpowiedzi immunologicznej i komunikacja międzykomórkowa. Limfocyty pośredniczą w adaptacyjnej odpowiedzi immunologicznej poprzez aktywność specyficzną dla antygenu.
Komórki plazmatyczne, których normalnie nie widać we krwi obwodowej, to zróżnicowane limfocyty B. Nie proliferują, są znacznie większe niż limfocyty B i mogą wydzielać duże ilości przeciwciał (2).
Widoczne mikroskopowo na rozmazie krwi limfocyty mają regularne, kuliste jądro i wysoki stosunek jądra do cytoplazmy. Cytoplazma, o zmiennej objętości, jest barwiona na jasnoniebieski kolor metodą Romanowskiego i jest albo przezroczysta, albo z nielicznymi, małymi, różowymi granulkami. Obecność granulek w większej komórce z większą ilością cytoplazmy może wskazywać na limfocyt T, ale do dalszego różnicowania różnych podtypów limfocytów wymagane jest immunofenotypowanie (3).
Pełna morfologia krwi (CBC) to wysoce zautomatyzowane badanie laboratoryjne, które generuje dane dotyczące wszystkich komórek krwi. Częścią morfologii krwi jest rozmaz białych krwinek, który identyfikuje i zlicza różne rodzaje prawidłowych komórek krwi, a także zapewnia dodatkowe pomiary i flagi dotyczące atypowych, nieprawidłowych i niedojrzałych białych krwinek.
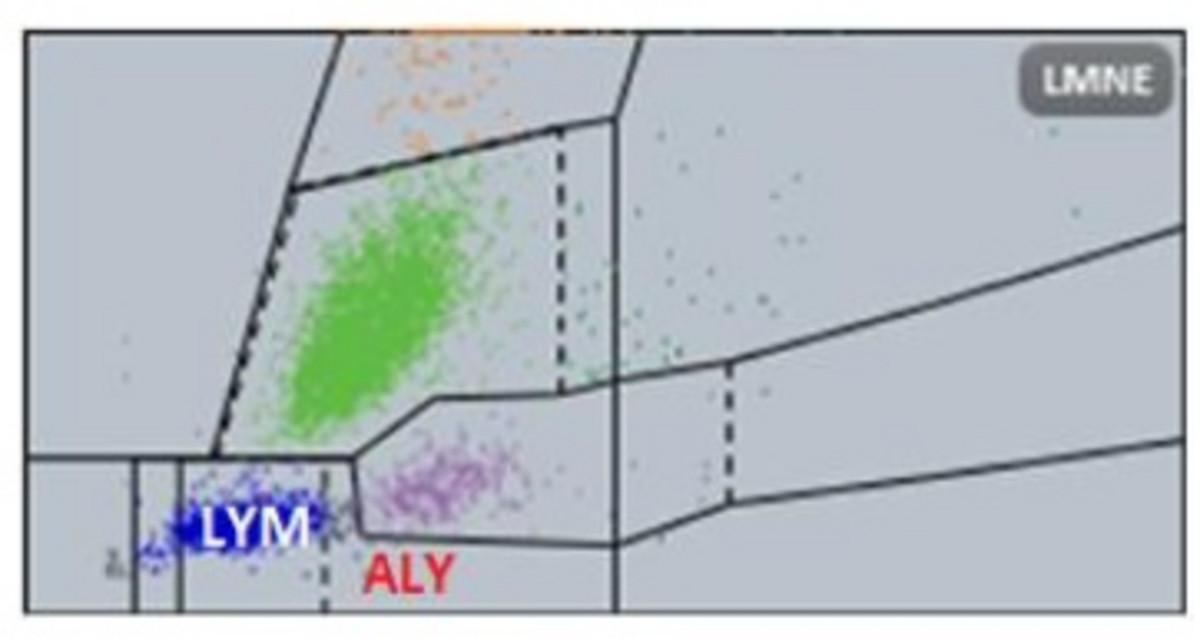
W analizatorach hematologicznych Yumizen białe krwinki można uwidocznić na scattergramie Diffa lub macierzy LMNE (rysunek 1). W tej macierzy ekstynkcja optyczna (oś Y) jest nanoszona na objętości (oś X), tworząc obraz z kilkoma skupiskami zdarzeń komórkowych. Macierz ma progi, niektóre stałe, a niektóre ruchome, co pozwala na określenie różnych populacji i wykrycie nieprawidłowości.
Rycina 1: Limfocyty (LYM) i ALY na matrycy LMNE
Dzięki tej precyzyjnej technologii analizatory hematologiczne Yumizen mogą definiować dwie dodatkowe populacje leukocytów istotne dla komórek limfocytarnych: duże niedojrzałe komórki (w tym niedojrzałe komórki limfoidalne – IML) i limfocyty atypowe (ALY), podawane zarówno w procentach, jak i w liczbach bezwzględnych.
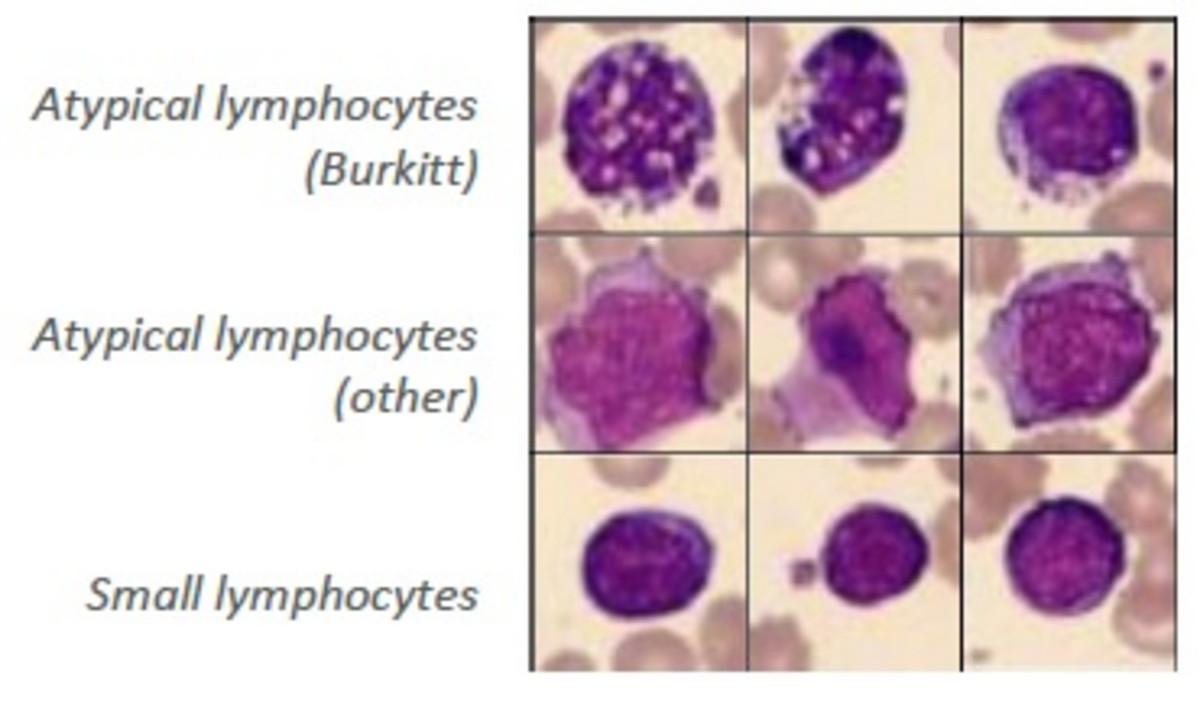
Limfocyty atypowe to limfocyty aktywowane w odpowiedzi na infekcję wirusową (czasami bakteryjną lub pasożytniczą). Komórki te charakteryzują się zwiększonym rozmiarem i często obecnością aktywnej syntezy białek, co powoduje pogłębienie niebieskiego zabarwienia cytoplazmy w barwieniu metodą Romanowskiego. Zwiększona aktywność może również powodować zmiany w jądrze, nadając mu bardziej otwarty wygląd z możliwą obecnością jąderek (4). Limfocyty różnią się szczegółami morfologicznymi, a także cechami markerów powierzchniowych, co wskazuje, że stanowią heterogeniczną mieszaninę typów komórek z poliklonalną odpowiedzią immunologiczną na stymulację antygenową. Limfocyty występują w wielu odmianach na rozmazach krwi. Patologicznie zmienione limfocyty są związane z wieloma chorobami. Na przykład w chłoniaku Burkitta można zaobserwować małe limfocyty i populację średniej wielkości komórek limfoidalnych o wysokiej aktywności proliferacyjnej i apoptotycznej (ryc. 2).
Rycina 2: Różne nietypowe limfocyty zidentyfikowane w rozmazie krwi barwionym MGG w przypadku chłoniaka Burkitta
W analizatorach hematologicznych Yumizen parametr ALY jest podawany wyłącznie do celów badawczych (RUO). Różne rodzaje komórek występujących w tym obszarze macierzy LMNE oraz ich specyficzność utrudniają określenie ostatecznych wartości odcięcia dla ALY. W zależności od obecnych komórek, może występować nakładanie się wartości ALY i IML dla dużej populacji niedojrzałych komórek (LIC).
Matryca wykorzystuje progowanie mobilne, aby zoptymalizować wychwyt populacji ALY. Chociaż obszar ten zazwyczaj reprezentuje duże aktywowane i reaktywne limfocyty, może również zawierać niewielkie blasty, komórki plazmatyczne oraz nieprawidłowe komórki chorób limfoproliferacyjnych, takie jak przewlekła białaczka limfocytowa (CLL), komórki Sezary'ego i tricholeukocyty (komórki włochate).
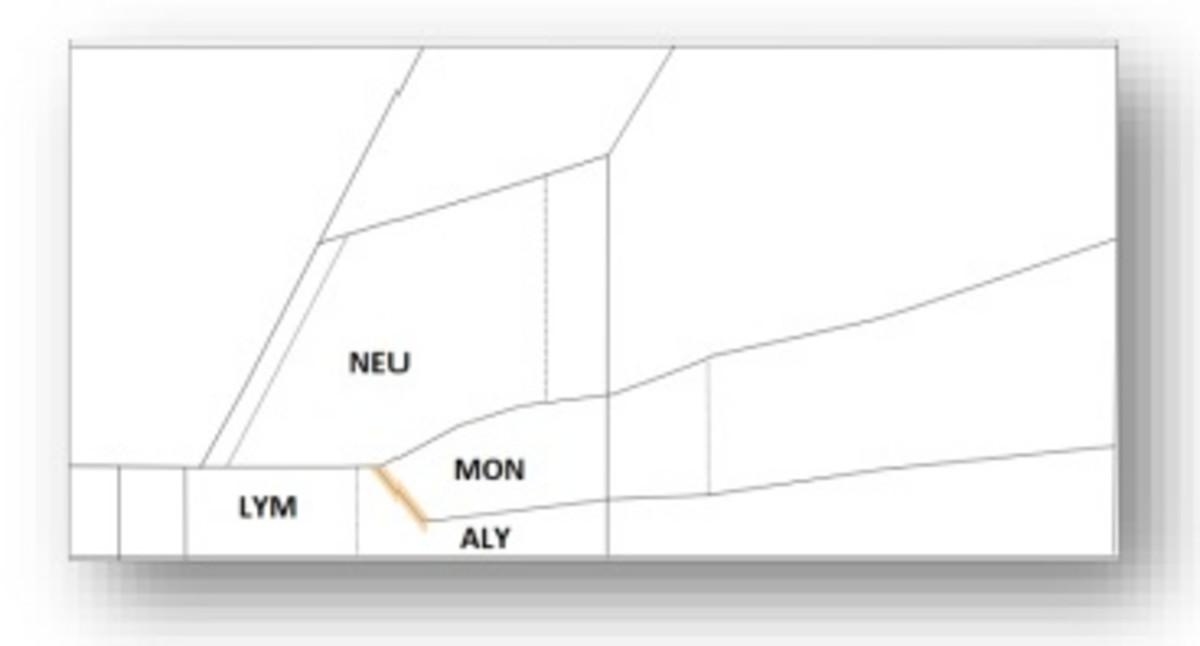
W przypadku populacji, które trudniej rozdzielić: limfocyty (LYM), monocyty (MON), neutrofile (NEU) i ALY (#, %) są oznaczane flagą podejrzenia, gdy nie zostanie znaleziony próg rozdziału między obszarami limfocytów i monocytów (alarm SepLymMon) (rysunek 3), co pozwala recenzentowi na podjęcie dalszych działań, takich jak badanie rozmazu krwi.
Rysunek 3: Próg separacji wyzwalający alarm ALY na matrycy LMNE
Chociaż ALY są nietypowe dla osób zdrowych, wyniki badań klinicznych są powszechnie interpretowane w odniesieniu do populacyjnych przedziałów referencyjnych. Dlatego przeprowadzono badanie przedziałów referencyjnych zgodnie z wytycznymi CLSI C28-A3 (Definiowanie, Ustalanie i Weryfikacja Przedziałów Referencyjnych w Laboratorium Klinicznym) dla parametru ALY na analizatorach Yumizen H2500 i H1500. Łącznie 240 próbek krwi pełnej (120 mężczyzn i 120 kobiet w wieku > 18 lat) pobranych na EDTA od pozornie zdrowych dawców rasy białej przeanalizowano w dwóch powtórzeniach na trzech analizatorach: dwóch Yumizen H2500 i jednym Yumizen H1500. Próbki przechowywano w temperaturze pokojowej między pobraniem a wykonaniem testu. Przedział referencyjny ustalono tak, aby obejmował dolną i górną granicę referencyjną, które obejmują 95% wartości uzyskanych od osób z populacji referencyjnej. Wyniki przedstawiono w Tabeli 1.
| Kobieta | Mężczyzna | Dane bibliograficzne (mężczyźni i kobiety) | |
| Dolna granica odniesienia (ALY%) | 0.20 | 0.20 | 0.00 |
| Górna granica odniesienia (ALY%) | 1.90 | 1.70 | 2.50 |
| Dolna granica odniesienia (ALY#) | 0.01 | 0.01 | 0.00 |
| Górna granica odniesienia (ALY#) | 0.14 | 0.09 | 0.20 |
Tabela 1: Dolne i górne granice odniesienia wyznaczone w badaniu dla parametru ALY w porównaniu do wartości z danych bibliograficznych (5, 6).
Obecność kilku atypowych limfocytów w większości próbek krwi prawdopodobnie ma niewielkie znaczenie kliniczne. Parametr ALY może jednak pomóc lekarzowi w postawieniu diagnozy lub wykorzystać go w celach prognostycznych. Limfocyty atypowe najczęściej występują w mononukleozie zakaźnej, toksoplazmozie, zapaleniu wątroby i innych infekcjach wirusowych.
Atypowe limfocyty obserwowano również we krwi obwodowej pacjentów w wielu innych sytuacjach klinicznych, w tym w reakcjach immunologicznych na przeszczep i szczepienie, kolagenozach i innych chorobach autoimmunologicznych, chorobach nowotworowych, reakcjach na leki, niektórych infekcjach bakteryjnych, lekach i stresie (7). W ostrej białaczce limfoidalnej (ALL) z małymi blastami, limfoblasty te często występują w obszarze ALY. Rysunek 4 przedstawia przykład ostrej białaczki limfoblastycznej z komórek T, w której populacja limfoblastów jest szczególnie obecna w obszarze atypowych limfocytów macierzy LMNE.
Rycina 4: Populacja limfoblastów w ostrej białaczce limfoblastycznej T (ALL T)
W przewlekłej białaczce limfatycznej na obszarze ALY wykresu DIFF można również zaobserwować limfocyty atypowe i niedojrzałe komórki limfocytarne (8).
Niewielka, zwarta populacja komórek blastycznych z ostrej białaczki szpikowej może występować w tym regionie ze względu na ich mniejsze rozmiary. W tym przypadku zwartą populację komórek blastycznych można zaobserwować na macierzy LMNE pomiędzy obszarami limfocytów, limfocytów atypowych i monocytów i odpowiednio oznaczyć ją flagą. Do monitorowania postępu danej infekcji, ALY mogą być stosowane jako narzędzie prognostyczne. Na przykład, atypowe limfocyty krążące we krwi odnotowano u pacjentów z COVID-19. Stwierdzono, że limfocyty reaktywne wobec COVID-19 są powiązane z lepszym rozwojem i rokowaniem choroby. Ich obecność sugeruje obfitą produkcję limfocytów T specyficznych dla wirusa, co wskazuje na lepsze rokowanie u pacjentów z tymi komórkami w krążeniu (9, 10).
Dzisiejsze analizatory wysokoprzepustowe zostały zaprojektowane tak, aby dostarczać jak najbardziej kompleksowych informacji o próbce. Dane te opierają się na wartościach progowych i złożonych algorytmach, a następnie muszą zostać starannie zinterpretowane przez lekarza. W tym kontekście parametr ALY dostarcza informacji, które mogą uzupełniać rutynowe parametry krwi i poprawiać obraz kliniczny pacjenta. Może być również przydatny w leczeniu choroby lub w celach prognostycznych.
1. HC Allen, P. Sharma. Histologia, Komórki plazmatyczne, 28 stycznia 2021 r.
2. R. Warrington, W. Watson, H. Kim i F. Antonetti, Wprowadzenie do immunologii i immunopatologii, Alergia, astma i immunologia kliniczna, tom 7, numer artykułu: S1 (2011)
3. A. Adewoyin i B. Nwogoh, Rozmaz krwi obwodowej – recenzja, Ann Ib Postgrad Med. grudzień 2014; 12 ust. 2: 71–79.
4. MW Simon, Limfocyt nietypowy, International Pediatrics, styczeń 2003 r. 18(1):20-22
5. C. Sultan / M. Gouault - Helman / M. Imbert, AIDE MEMOIRE D'HEMATOLOGIE. Service Central d'Hématologie de l'Hôpital Henri Mondor, Faculté de médecine de Créteil (Paryż XII). 1998 Troussard X, tom S,
6. E. Cornet, V. Bardet, JP. Couaillac, C. Fossat, JC. Luce, E Maldonado, V. Siguret, J. Tichet, O. Lantieri, J. Corberand. Normalne wartości referencyjne pełnej morfologii krwi dla dorosłych we Francji. Journal of Clinical Pathology (2014) 67 (4): 341-4.
7. T. Shiftan, J. Mendelsohn, Krążący „atypowy” limfocyt, Human Pathology, styczeń 1978;9(1):51-61
8. Horiba Medical: Studium przypadku klinicznego. Yumizen H1500/H2500
9. A. Merino, J. Rodellar i wsp., Atypowe komórki limfoidalne krążące we krwi w zakażeniu COVID-19: morfologia, immunofenotyp i wartość prognostyczna. Journal of Clinical Pathology, grudzień 2020: jclinpath-2020-207087.
10. D. Gérard, S. Henry, B. Thomas, SARS-CoV-2: nowa etiologia atypowych limfocytów, Images In Haematology, 20 kwietnia 2020 r.
Globalne rozwiązanie hematologiczne
Analizator Hematologiczny
Analizator Hematologiczny
Analizator Hematologiczny
Analizator Hematologiczny
Analizator Hematologiczny
Masz pytania lub prośby? Skorzystaj z tego formularza, aby skontaktować się z naszymi specjalistami.