Płytki krwi, czyli trombocyty, to dyskowate fragmenty cytoplazmy, zazwyczaj obecne we krwi obwodowej. Krążące płytki krwi są produkowane z megakariocytów, głównie w szpiku kostnym. Dojrzałe płytki krwi, choć niewielkie, zazwyczaj o objętości od 2 do 20 flL, w porównaniu z erytrocytami lub leukocytami, odgrywają ważną rolę zarówno w hemostazie pierwotnej, jak i w czynnikach krzepnięcia, a także w reakcji zapalnej organizmu.
Ilościowe i jakościowe zaburzenia płytek krwi są powszechne, a liczba płytek krwi ma kluczowe znaczenie w ocenie ryzyka wystąpienia samoistnego krwawienia u danego pacjenta. Stężenie płytek krwi (PLT) jest podstawowym parametrem pełna morfologia krwi (CBC). Wskaźniki płytkowe (PI) — płytkokryt (PCT), średnia objętość płytek krwi (MPV), szerokość rozkładu wielkości płytek krwi (PDW) i stosunek płytek krwi do dużych komórek (P-LCR) — to grupa pochodnych parametrów płytek krwi uzyskiwanych w ramach automatycznej morfologii krwi. Średnią objętość płytek krwi (MPV) oblicza się, dzieląc płytkokryt (PCT), analogiczny do hematokrytu krwinek czerwonych, przez liczbę płytek krwi (1). MPV, mierzony za pomocą automatycznych analizatorów krwi, odzwierciedla średnią wielkość płytek krwi w krążeniu. Wiadomo, że wskazuje on na przyspieszoną syntezę płytek krwi przez szpik kostny w odpowiedzi na zwiększone niszczenie płytek krwi na obwodzie (2). PDW to szerokość krzywej rozkładu wielkości płytek krwi (3). Wskaźnik płytek krwi do dużych komórek (P-LCR) definiuje się jako odsetek płytek krwi, których objętość przekracza prawidłową wartość 12 fL w całkowitej liczbie płytek krwi. Jest on obliczany w automatycznych analizatorach krwi według wzoru:
P-LCR = P-LCC/PLT, gdzie P-LCC to liczba dużych płytek krwi. Wykazano, że rozmiar płytek krwi odzwierciedla ich aktywność; dlatego MPV (średnia objętość płytek krwi) i P-LCR to prosta i łatwa metoda pośredniej oceny stymulacji płytek krwi.
Cztery główne metody liczenia płytek krwi to: ręczna – mikroskopia fazowo-kontrastowa, impedancyjna, rozpraszanie światła optycznego/fluorescencja i cytometria przepływowa, liczenie immunologiczne.
Do niedawna ręczna metoda liczenia płytek krwi stanowiła punkt odniesienia, z którym porównywano wszystkie metody automatyczne. Chociaż jest czasochłonna, nadal jest wykonywana w rutynowym laboratorium w przypadku niskiej liczby płytek krwi lub obecności płytek nietypowych w próbce. Wprowadzenie automatycznych liczników pełnej krwi spowodowało znaczną poprawę precyzji i znacząco skróciło czas analizy w porównaniu z metodą ręczną. Jednak liczniki automatyczne mają swoje ograniczenia, a dzisiejszą metodą odniesienia w liczeniu płytek krwi jest połączenie cytometrii przepływowej fluorescencyjnej i liczenia metodą impedancji aperturowej (4).
W metodzie impedancyjnego zliczania płytek krwi komórki są traktowane jako całkowicie nieprzewodzące cząstki rezystywności. Gdy krwinka zawieszona w roztworze elektrolitu przechodzi przez strefę pomiarową apertury, obserwuje się wykrywalną zmianę impedancji elektrycznej proporcjonalną do objętości komórki. Każda pojedyncza komórka generuje sygnał impedancji, który jest proporcjonalny do objętości wykrytej komórki. Wykorzystując tę zależność między sygnałem impedancji a rozmiarem komórki/cząstki, komórki/cząstki są dalej dzielone na dwie kategorie komórkowe:
• Małe komórki – od 2 do 30 fL – odnoszące się do płytek krwi
• Większe komórki – od 30 do 200 fL – w odniesieniu do zakresu liczenia czerwonych krwinek (RBC).
Istotną wadą metody impedancji elektrycznej w liczeniu płytek krwi jest trudność w odróżnianiu dużych płytek od skrajnie mikrocytowych lub pofragmentowanych krwinek czerwonych, pofragmentowanych, pozbawionych jąder krwinek białych i innych cząstek o podobnej wielkości, co skutkuje fałszywym wzrostem raportowanej liczby płytek krwi. Trudność ta wynika z dyskryminatora stosowanego w oparciu o rozmiar do oddzielenia płytek krwi od erytrocytów. I odwrotnie, w przypadku próbek zawierających duże płytki krwi, a także skupiska płytek o wielkości > 30 fl (jak obserwowano w przypadku aglutynin EDTA-zależnych), raportowany będzie fałszywy spadek. Wreszcie, możliwe jest znaczne zróżnicowanie powtarzalności wyników między różnymi analizatorami ze względu na różnice w technikach analitycznych stosowanych przez różnych producentów.
Niedawno wprowadzono metody optycznego rozpraszania światła do liczenia płytek krwi. Komórki w odpowiednim rozcieńczalniku przechodzą przez wąską wiązkę światła (tj. laser helowo-neonowy). Oświetlenie i rozproszenie światła przez każdą komórkę mierzy się pod jednym kątem (jednowymiarowo) lub pod dwoma kątami (dwuwymiarowo) rozpraszania światła. Objętość i współczynnik załamania światła poszczególnych płytek krwi są jednocześnie określane dla każdej komórki z osobna. Dwa pomiary rozproszenia są przekształcane na wartości objętości (rozmiaru płytki krwi) i współczynnika załamania światła (gęstości płytek krwi) przy użyciu teorii rozpraszania światła Mie dla jednorodnych sfer. Następnie, zintegrowana analiza jest wykorzystywana do rozróżnienia płytek krwi, dużych płytek krwi, krwinek czerwonych, fragmentów komórek i resztek (5). Płytki krwi są identyfikowane na mapie na cytogramie rozproszenia płytek krwi na podstawie ich objętości i współczynnika załamania światła (1,35–1,40).
W fluorescencyjnym zliczaniu płytek krwi barwnik polimetinowy służy do barwienia RNA/DNA komórek siateczkowatych oraz błony i granulek płytek krwi. Wewnątrz kuwety przepływowej każda pojedyncza komórka jest przepuszczana przez wiązkę światła lasera diodowego półprzewodnikowego. Technologia ta umożliwia jednoczesne zliczanie retikulocytów, erytrocytów i fluorescencyjnych płytek krwi. Analizowana jest intensywność fluorescencji każdej komórki, co pozwala na oddzielenie płytek krwi od krwinek czerwonych i retikulocytów.
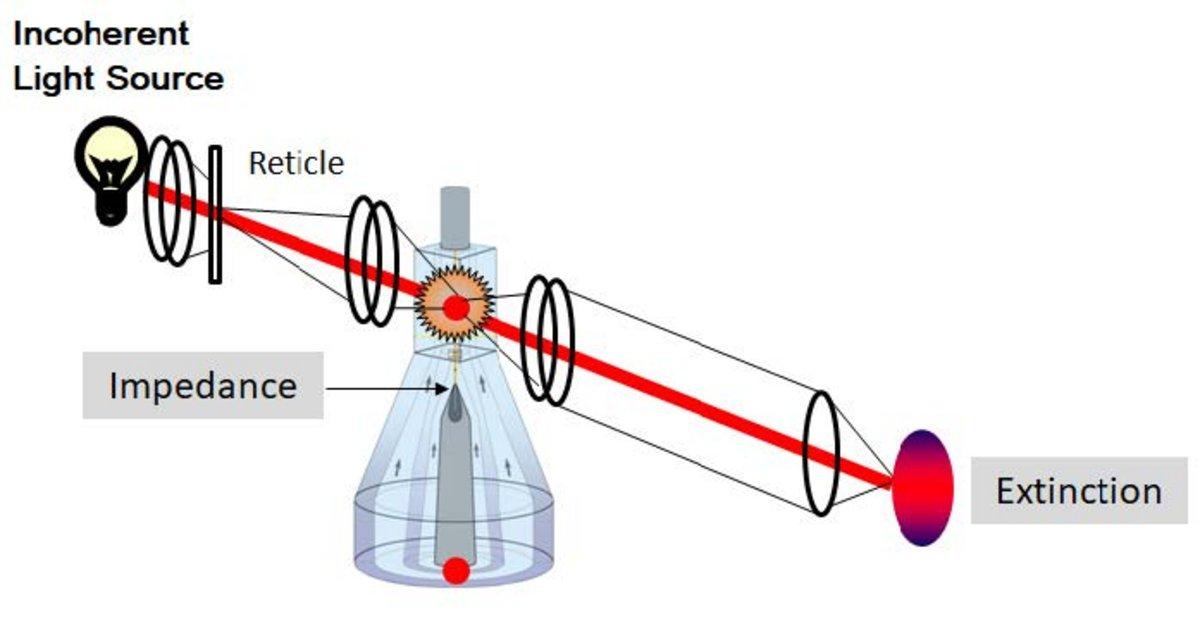
W trybie PLTOx analizatorów Yumizen, w celu uzyskania najbardziej wiarygodnego wyniku, łączone są dwie metody pomiaru – impedancji i wygaszenia światła (absorbancji) (rysunek 1).
Rysunek 1: HORIBA Medical płytki optyczne metoda pomiaru z użyciem niespójnego źródła światła
Zasada pomiaru jest podobna do metody LMNE. Po rozcieńczeniu próbki, roztwór przechodzi przez otwór kuwety przepływowej LMNE i okienko optyczne. W każdej kuwecie mierzona jest zarówno rezystywność (objętość), jak i ekstynkcja optyczna (cytochemia). Gęstość płytek krwi, czyli współczynnik załamania światła, określa stopień rozpraszania światła, a tym samym absorbancję lub ekstynkcję optyczną. Na podstawie tych pomiarów tworzona jest matryca z objętościami na osi X i absorbancją optyczną na osi Y (rysunek 2).
Rysunek 2: Wyświetlana macierz do różnicowania PLT/RBC na podstawie pomiaru optycznego
Ponieważ pomiary impedancji i optyczne każdej komórki są wykonywane z opóźnieniem, istnieje algorytm asocjacyjny, który łączy oba pomiary. Pozwala to na uzyskanie reprezentacji macierzowej podobnej do scattergramu. Reprezentacja macierzowa pozwala na lepszą klasyfikację, gdy populacje nakładają się na siebie w jednym lub obu pomiarach. Światło wygaszania jest wrażliwe na współczynnik załamania światła, co pozwala na odróżnienie PLT od RBC o tej samej wielkości (rysunek 2). Jednocześnie instrument przeprowadza cykl RBC/PLT Low-Value.
Parametr PLTOPT odpowiada procentowej liczbie płytek krwi w stosunku do liczby erytrocytów zidentyfikowanych na matrycy, pomnożonej przez liczbę erytrocytów zidentyfikowanych w komorze pomiarowej. Nie ma potrzeby indywidualnej kalibracji tego parametru, ponieważ opiera się on na kalibracji erytrocytów.
Technologia pomiaru ekstynkcji płytek krwi HORIBA wykorzystuje niespójne źródło światła (źródło rozszerzone). Wysoka apertura numeryczna wiązki światła umożliwia obserwację komórek pod różnymi kątami, ukazując z jednej strony morfologię poszczególnych przedziałów komórkowych, a z drugiej – charakterystykę spektroskopową wewnątrzcytoplazmy.
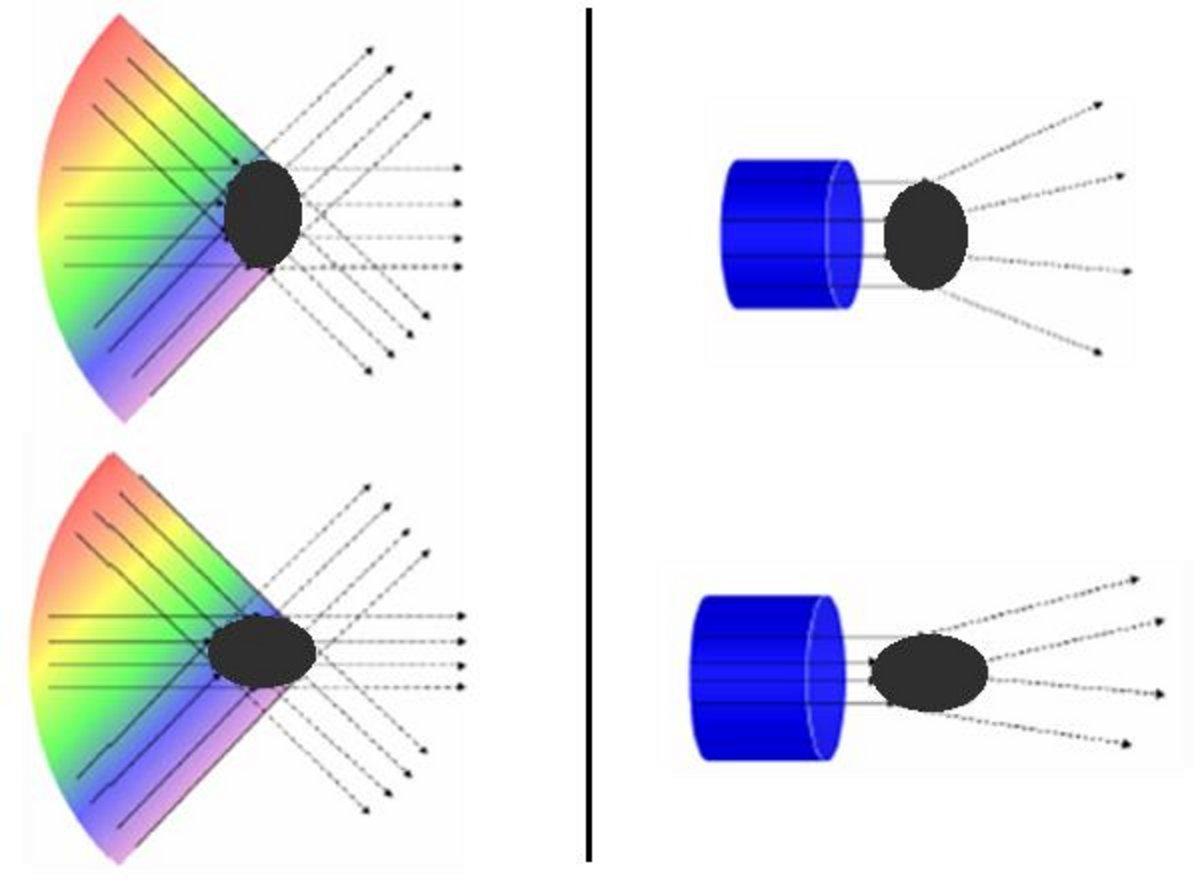
W przeciwieństwie do monochromatycznego światła laserowego generującego idealnie równoległą wiązkę i w konsekwencji umożliwiającego obserwację komórki z jednego wymiaru, pomiar wykonany przy użyciu niespójnego źródła światła jest mniej podatny na anizotropię komórki oraz jej położenie lub orientację w wiązce i dostarcza informacji zależnych od wewnętrznych cech komórki (rysunek 3).
Rysunek 3: Rozpraszanie widmowe światła (po lewej) w porównaniu z rozpraszaniem generowanym laserowo (po prawej)
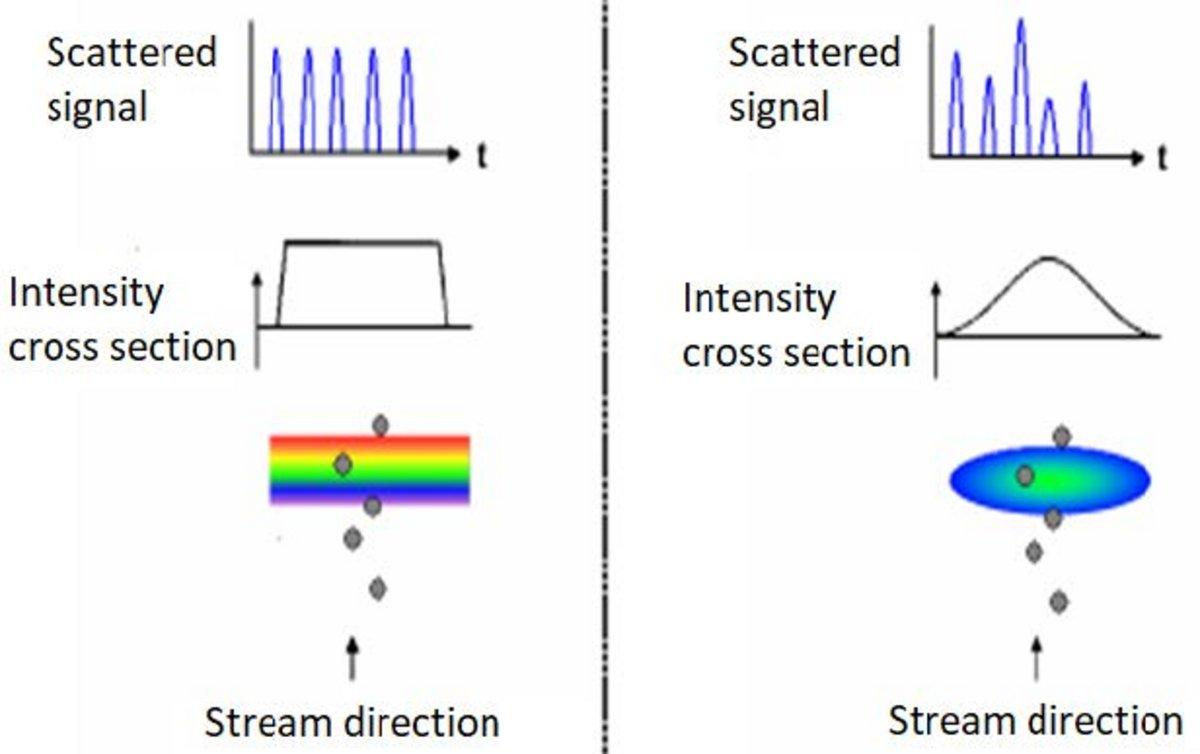
W przypadku spektralnego źródła światła, takiego jak monochromatyczne światło laserowe, sygnał związany z charakterystyką komórki jest silnie zależny od położenia i orientacji komórki w punkcie pomiarowym i musi być wyśrodkowany na osi. W przeciwnym razie odpowiedź świetlna może być zniekształcona i dawać różne wyniki, jak pokazano na rysunku 4.
Rysunek 4: Rozpraszanie widmowe światła (po lewej) w porównaniu z rozpraszaniem generowanym laserowo (po prawej)
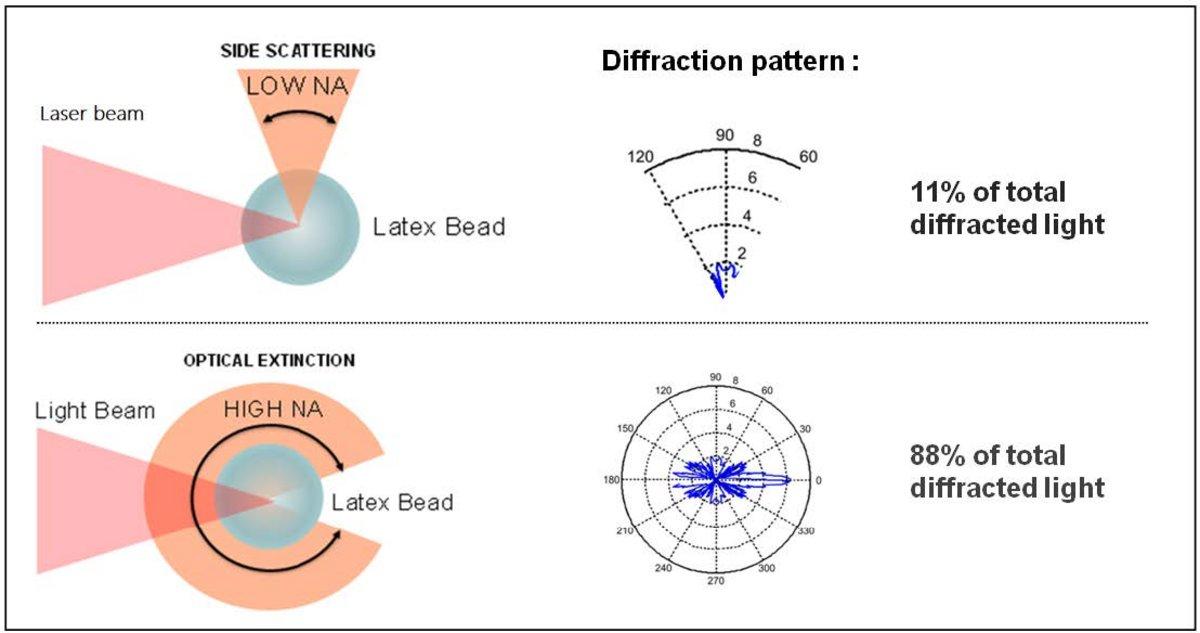
Gdy światło pada na komórkę, ulega ono dyfrakcji w specyficzny sposób. Właściwości rozpraszania światła są związane z morfologią komórki. Apertura numeryczna (NA) układu optycznego jest miarą jego kątowej akceptacji padającego światła. W badaniu PLT z wykorzystaniem technologii laserowej, apertura numeryczna (NA) jest mniejsza i odpowiada około 11% całkowitego światła dyfrakcyjnego. W przypadku technologii światła niespójnego HORIBA, większa apertura numeryczna (NA) daje światło dyfrakcyjne odpowiadające około 88% całkowitego światła dyfrakcyjnego (rysunek 5); analiza jest zatem znacznie lepsza i dokładniejsza.
Zasada liczenia immunologicznego polega na znakowaniu krwi z antykoagulantem EDTA odpowiednim monoklonalnym przeciwciałem przeciwpłytkowym sprzężonym z fluoroforem (tj. izotiocyjanianem fluoresceiny FITC). Opisano wiele takich przeciwciał, w tym anty-CD42a; anty-CD41b; anty-CD61; oraz anty-CD41, anty-CD42 i anty-CD61.
Rysunek 5: Technologie laserowe i wiązki światła niespójnego oraz odpowiadające im apertury numeryczne (NA) i wzory dyfrakcyjne
Próbka jest następnie analizowana za pomocą cytometru przepływowego. Metoda ta pozwala określić liczbę płytek krwi na podstawie stosunku płytek fluorescencyjnych do czerwonych krwinek w próbce. Immunologiczne liczenie płytek krwi za pomocą cytometru przepływowego jest dokładne i wiarygodne; jednak technika ta byłaby bardzo kosztowna, gdyby zastosować ją do wszystkich próbek w w pełni zautomatyzowanym liczniku krwinek.
W celu określenia wartości materiałów kalibracyjnych i kontrolnych analizatora hematologicznego Międzynarodowa Rada Normalizacji w Hematologii (ICSH) oraz Międzynarodowe Towarzystwo Hematologii Laboratoryjnej (ISLH) zalecają liczenie specjalnie znakowanych płytek krwi w odniesieniu do erytrocytów za pomocą cytometru przepływowego z fluorescencją, wraz z dokładnym zliczaniem erytrocytów określonym za pomocą półautomatycznego licznika impedancji apertury jednokanałowego jako metody odniesienia do zliczania płytek krwi.
Dlatego też, aby uzyskać najbardziej wiarygodne wyniki, łączy się kilka metod i technologii. Świeże próbki krwi żylnej z antykoagulantem EDTA są mierzone w ciągu 4 godzin od pobrania. Próbka jest wstępnie rozcieńczana, a płytki krwi znakowane dwoma przeciwciałami monoklonalnymi specyficznymi dla klastra różnicowania (CD) wspólnego dla wszystkich płytek krwi. Przynajmniej 50 000 zdarzeń z minimalną liczbą 1000 zdarzeń płytkowych jest liczonych za pomocą cytometru przepływowego w celu określenia stosunku RBC/płytki krwi. Liczbę płytek krwi oblicza się następnie na podstawie tego stosunku i stężenia RBC w oryginalnej próbce krwi (6).
Płytki krwi to złożone składniki krwi o zróżnicowanych funkcjach. Ich liczba, kształt, objętość i pochodne wskaźniki płytkowe są markerami różnych stanów patologicznych (7, 8). Technologie zliczania płytek krwi ewoluowały z biegiem czasu, a obecna metoda zliczania referencyjnego łączy w sobie kilka technologii. Ze względu na cenę i ograniczony dostęp do tych technologii, metoda zliczania referencyjnego nie może być stosowana do wszystkich próbek w rutynowej analizie.
Dzięki unikalnej technologii światła niespójnego, połączonej z pomiarem impedancji i czytelną macierzową reprezentacją stosunku RBC/PLT, analizatory HORIBA zapewniają optymalne rozwiązanie, możliwie najbliższe metodzie referencyjnej, w tej wieloaspektowej rutynowej analizie.
1. YU Budak, M. Polat i K. Huysal: Zastosowanie wskaźników płytkowych, plateletkrytu, średniej objętości płytek krwi i szerokości rozkładu płytek krwi w nagłych nieurazowych zabiegach chirurgicznych jamy brzusznej: przegląd systematyczny, Biochem Med (Zagrzeb). 2016 czerwca 10; 26(2): 178–193.
2. JD Bessman: Związek ploidii megakariocytów z objętością płytek krwi, American Journal of Hematology, luty 1984; 16(2):161-70.
3. D. Schmoeller, MM Picarelli, T. Paz Munhoz, CE Poli de Figueiredo i H. Luiz Staub: Średnia objętość płytek krwi i frakcja niedojrzałych płytek krwi w zaburzeniach autoimmunologicznych; Granice w medycynie, 06 września 2017 r
4. P. Harrison, K. Ault, S. Chapman, L. Charie, B. Davis, K. Fujimoto, B. Houwen, J. Kunicka, F.Lacombe, S. Machin, R. Raynor, L. van Hove, O. van Assendelft,, An interlaboratory study of acandidate referencyjna metoda zliczania płytek krwi. Amerykański dziennik patologii klinicznej.2001Mar; 115(3):448-59.
5. C. Briggs, P. Harrison i SJmachin: Ciągły rozwój zautomatyzowanego liczenia płytek krwi; International Journal of Laboratory Hematology, 2007, 29, 77–91.
6. Międzynarodowa Rada Normalizacji w Hematologii, Panel Ekspertów ds. Cytometrii* oraz Zespół Roboczy Międzynarodowego Towarzystwa Hematologii Laboratoryjnej ds. Liczenia Płytek Krwinek†. Liczenie płytek krwi metodą stosunku RBC/Platelet Ratio. Am J Clin Pathol 2001; 115:460-464
7. P. Harrison, C. Briggs, S. Machin: Postępy w liczeniu płytek krwi, Hematologia. 2001;5(6):421-7.
8. AY Gasparyan, L. Ayvazyan, DP Mikhailidis, GD Kita: Średnia objętość płytek krwi: związek między zakrzepicą a stanem zapalnym?; Current Pharmaceutical Design. 2011;17(1):47-58.
Analizator Hematologiczny
Analizator hematologiczny i OB
Masz pytania lub prośby? Skorzystaj z tego formularza, aby skontaktować się z naszymi specjalistami.