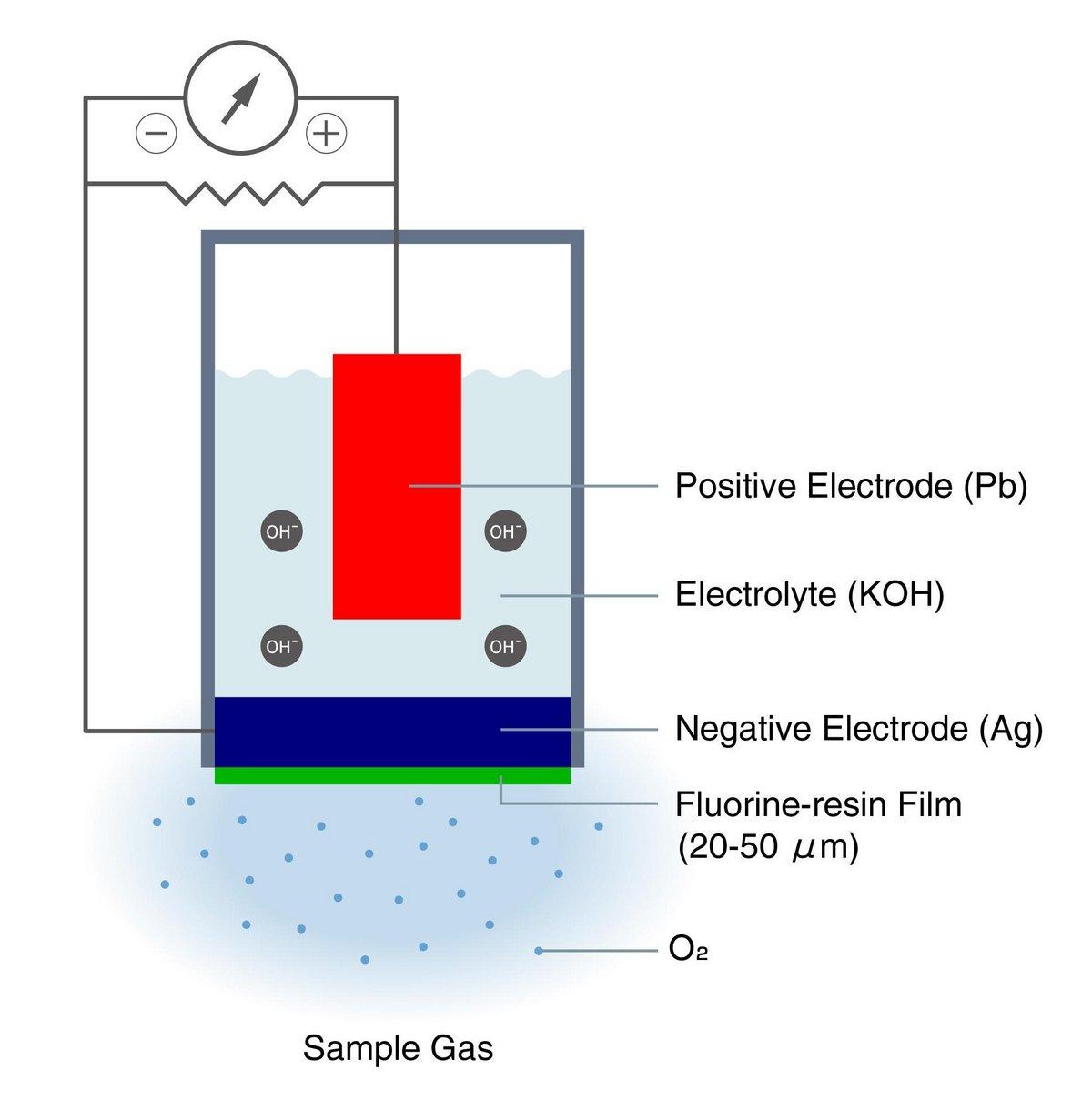
Figura 5: Estructura y principio de funcionamiento del método de celda electroquímica del analizador de oxígeno de tipo celda galvánica
Cuando un metal soluble en un electrolito (metal base como electrodo positivo de la celda) y un metal insoluble (metal precioso como electrodo negativo de la celda) se sumergen en el electrolito, el metal se disuelve en el electrodo positivo y libera electrones, que llegan al electrodo negativo. En el electrodo negativo, el oxígeno que atraviesa la película delgada absorbe electrones. (celda galvánica)
Reacción en el electrodo positivo y el electrodo negativo
Electrodo positivo
2Pb + 4OH-→ 2PbO + 2H2 O + 4e-
Electodo negativo
O2 + 2H2 O + 4E-→ 4OH-
Dado que la corriente por este flujo de electrones es proporcional al oxígeno que atraviesa la película delgada, la concentración de oxígeno se puede obtener midiendo esta corriente.
La figura 5 muestra un analizador de oxígeno tipo celda galvánica típico que utiliza hidróxido de potasio (KOH) como electrolito, plomo (Pb) como electrodo positivo, plata (Ag) como electrodo negativo y una película de resina de flúor como película delgada que permea el oxígeno.
El analizador de celda galvánica se puede utilizar para la medición continua de oxígeno en diversos procesos, incluso cuando coexisten gases inflamables o corrosivos en el gas de muestra. Además de la medición de gases, se utiliza para la medición continua de oxígeno disuelto en agua y líquidos.
Tabla de contenido
Tiene alguna pregunta o solicitud? Utilice este formulario para ponerse en contacto con nuestros especialistas.