

O tamanho importa nos sistemas de administração de vacinas. Nanopartículas menores que 200 nm geralmente apresentam uma resposta imunogênica maior do que micropartículas maiores que 1 mícron. Essa afirmação, bastante simples, baseia-se no entendimento comum de que partículas com tamanhos semelhantes às dimensões dos vírus são tratadas como vírus pelo organismo. No caso da fabricação da nova vacina contra a COVID-19, adenovírus com tamanho semelhante ao do SARS-CoV-2 (mediana de aproximadamente 90-100 nanômetros) são manipulados como carreadores (ou vetores virais) para desencadear a produção de proteínas spike. Em contrapartida, a literatura publicada demonstra que o efeito de vacinas administradas por via oral, intranasal ou por outras superfícies mucosas favorece formulações microparticuladas em relação às nanoparticuladas, devido à maior carga antigênica. O tamanho das impurezas também afeta significativamente a eficácia da vacina. Em suma, muitos ingredientes de formulações de vacinas devem ter tamanho, distribuição de tamanho e quantidade de partículas controlados ao longo de todo o processo de desenvolvimento, fabricação, armazenamento e administração.
O processo inicial de preparação de vacinas exige uma caracterização cuidadosa do vírus para alcançar infectividade e estabilidade otimizadas. Os títulos infecciosos são usados para determinar a concentração de partículas virais capazes de transduzir células e sua carga viral em uma amostra. Duas técnicas analíticas consagradas para medir títulos infecciosos são:
Ambas as abordagens quantificam a quantidade de vírus presente em uma solução. O ensaio de placas virais para lentivírus, por exemplo, requer até duas semanas de incubação para determinar o resultado em Unidades Formadoras de Placas (UFP) por mL. A contagem de UFP também é subjetiva, resultando em baixa reprodutibilidade entre diferentes analistas. A qPCR, por outro lado, não discrimina entre vírus inteiros, fragmentados, vazios, agregados, infecciosos ou não infecciosos; ela apenas determina a expressão gênica viral relativa e correlaciona o valor com as UFP. A desvantagem é que a qPCR requer conhecimento prévio da sequência do genoma viral, pode ser dispendiosa e analisa a concentração de material genômico, não de vírus infecciosos, uma vez que RNA ou DNA não revestidos podem estar presentes em uma amostra, mas, sem o revestimento, são incapazes de entrar em uma célula.
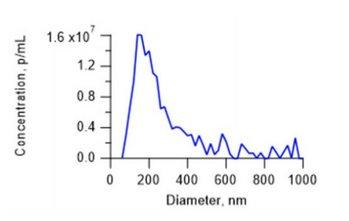
Figura 1: Resultado da medição de uma amostra de vetor viral humano. Observe a distribuição que exibe a presença tanto de detritos celulares do hospedeiro quanto de agregados.
Os resultados da análise de concentração de partículas obtidos com o sistema de rastreamento de nanopartículas (NTA) multilaser ViewSizer 3000™ correlacionam-se com as Unidades Formadoras de Placa (UFP), de forma semelhante à qPCR. Graças à operação simultânea de três lasers, o sistema quantifica não apenas as partículas virais intactas, mas também os agregados infecciosos. A Figura 1 demonstra a distribuição de tamanho das partículas de uma amostra de vetor viral humano, um vírus candidato utilizado na fabricação de vacinas. Observe a população significativa de partículas maiores.
Baixe a Nota Aplicação 227: Obtendo Título Infeccioso com Análise de Rastreamento de Nanopartículas (NTA) com múltiplos lasers
A capacidade de analisar eficazmente toda a gama de tamanhos permite ao ViewSizer 3000 correlacionar com sucesso o título infeccioso conhecido com a concentração total de partículas, com um valor R² superior a 0,9, comprovando que a técnica NTA multi-laser é uma alternativa nova, económica e eficiente em termos de tempo, em comparação com a VPA e a qPCR.
Assista ao webinar sob demanda: Concentração e tamanho de vírus e partículas semelhantes a vírus.
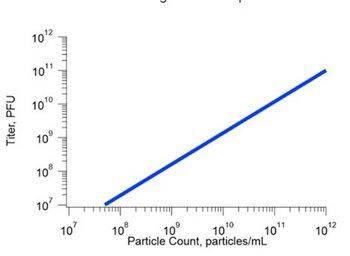
Figura 2: Correlação do título infeccioso.
Partículas semelhantes a vírus (VLPs, na sigla em inglês) são projetadas para imitar o vírus de interesse e provocar um efeito terapêutico (como imunidade) sem o custo do vírus ou o risco de infecção. Elas têm sido o foco de inúmeras pesquisas sobre vacinas inovadoras. O tamanho das VLPs é semelhante ao dos vírus, que normalmente varia de algumas dezenas a algumas centenas de nanômetros. Além da técnica NTA multilaser ViewSizer 3000, o analisador de tamanho de partículas por difração a laser LA-960V2 também é adequado para a análise de VLPs. A difração a laser é uma técnica de conjunto que permite análises rápidas e rotineiras. A técnica também é fundamentalmente mais sensível a partículas maiores, como contaminantes. Dependendo de como a VLP é fabricada, fragmentos do material inicial provavelmente estarão presentes na amostra em tamanhos maiores do que a própria VLP. Isso ocorre quando materiais (como emulsões) são preparados com uma distribuição de tamanho ampla e, em seguida, o tamanho é reduzido para produzir um produto final. Partículas grandes remanescentes podem levar a uma resposta imune indesejada ou a problemas de filtração em processamentos subsequentes (como a esterilização por filtração). Para analisar vírus e VLPs, é essencial uma técnica que abranja uma ampla faixa dinâmica de partículas.
Um exemplo de resultado de tamanho (abaixo da Figura 3) mostra três populações distintas. A população mais fina (menor tamanho de partícula) é a própria VLP. As populações restantes (com diâmetros acima de cerca de 1 mícron) são o material inicial que ainda não foi triturado ou moído para tamanhos mais finos. O LA-960V2 pode fornecer métricas de tamanho para toda a população, bem como métricas para cada população individual, usando o Relatório Multimodal.
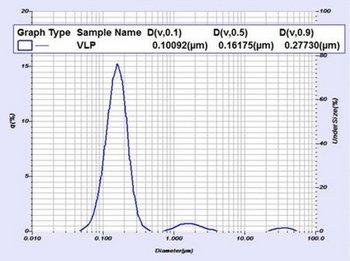
Figura 3: Distribuição do tamanho de partículas e resultados para um material VLP medido pelo LA-960. Esta amostra mostra três populações distintas. A população mais fina (menor tamanho de partícula) é o próprio VLP. As populações restantes (com diâmetros acima de cerca de 1 mícron) são material inicial que ainda não foi cisalhado ou moído para tamanhos mais finos.
Assista ao webinar sob demanda: [Universidade de Maryland] Injeção intralinfática de depósitos de liberação controlada para potencializar a vacinação e modular a resposta imune.
Um subgrupo de vesículas extracelulares (VE) conhecidas como exossomos desempenha um papel cada vez mais importante e complexo no diagnóstico e tratamento de diversas doenças. São responsáveis pela transferência de material genético e pela comunicação intercelular, transportando diversos ácidos nucleicos, incluindo RNA, lipídios e proteínas. Suas propriedades imunogênicas, segundo diversos estudos publicados, correlacionam-se com a quantidade de antígenos associados, criando, assim, uma oportunidade para o desenvolvimento de potenciais vacinas.
O tamanho e a concentração das partículas de exossomos são especialmente analisados, pois fornecem informações clínicas importantes. Até o momento, no entanto, a pesquisa sobre vesículas extracelulares (VEs) ainda carece de padronização para o processo de purificação. Além disso, tem sido limitada pelas tecnologias analíticas utilizadas para medi-las. Sabe-se, porém, que as VEs são um grupo heterogêneo de partículas com uma variedade de tamanhos e biogênese; espera-se que a distribuição de tamanho seja ampla, mesmo após o processamento.
Assista ao webinar sob demanda: Exossomos: Explorando o Potencial Diagnóstico e Terapêutico das Nanopartículas Biológicas da Natureza
O ViewSizer 3000 possui três lasers operando simultaneamente em 635 nm (vermelho), 520 nm (verde) e 445 nm (azul), além de uma câmera colorida para visualizar com precisão partículas de grande faixa dinâmica. Ele supera a desvantagem comum da NTA convencional, que é a dificuldade em dimensionar partículas com precisão em amostras polidispersas. Amostras de exossomos de pré-adipócitos humanos (células-tronco mesenquimais) (100 µg) adquiridas da ZenBio foram analisadas utilizando o ViewSizer 3000. O resultado foi validado por uma técnica de sensoriamento resistivo ajustável e apresentou um perfil com diâmetro de partícula D50 de 148 nm e concentração total de partículas de 5,7 x 10⁷ partículas/mL.
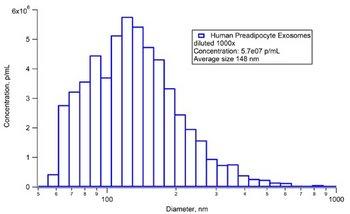
Figura 4: Distribuição do tamanho e da concentração das partículas de exossomos.
Baixe a Nota Aplicação 218: Distribuição do Tamanho de Partículas e Concentração de Exossomos
Vírus, VLPs (como adjuvantes) e exossomos podem ser analisados quanto ao tamanho e concentração usando um instrumento de análise de rastreamento de nanopartículas (NTA) com múltiplos lasers, o ViewSizer 3000. A maioria das amostras apresenta uma ampla distribuição de tamanho que dificulta a análise NTA com um único laser. Se apenas a distribuição de tamanho for necessária, como em um processo de redução de tamanho, a difração a laser também se mostrou útil.
Análise simultânea de rastreamento de nanopartículas multiespectrais (NTA)
Analisador de Distribuição de Tamanho de Partículas por Dispersão de Laser
Você tem alguma dúvida ou solicitação? Utilize este formulário para entrar em contato com nossos especialistas.