
Las modificaciones en la superficie del SPRi-Biochip (a unos 200 nm), como una interacción entre ligandos y analitos, inducen un cambio en las condiciones de resonancia, que pueden medirse.
La resonancia plasmónica superficial (SPR) es un proceso de detección óptica que puede ocurrir cuando la luz polarizada impacta en un prisma cubierto por una fina capa metálica. Bajo ciertas condiciones (longitud de onda, polarización e ángulo de incidencia), los electrones libres en la superficie metálica del SPRi-Biochip absorben fotones de luz incidente y los convierten en ondas plasmónicas superficiales. Estas ondas penetran el medio sobre la superficie a unos 100 a 200 nm. A un ángulo de incidencia específico (llamado ángulo de resonancia), las ondas plasmónicas resuenan con la luz incidente, lo que provoca una caída de la reflectividad. Las curvas de plasmón muestran las variaciones de la luz reflejada recogida en la cámara frente al ángulo de incidencia. La posición del ángulo de resonancia es muy específica del entorno local de la superficie del SPRi-Biochip.
Las modificaciones en la superficie del SPRi-Biochip (a unos 200 nm), como una interacción entre ligandos y analitos, inducen un cambio en las condiciones de resonancia, que pueden medirse.
Un plasmón es el fenómeno físico que caracteriza la oscilación del plasma. Más precisamente, en física, de la misma manera que los fotones son la cuantificación de ondas de luz, un plasmón es un cuántico de oscilación del plasma. El plasmón es la cuasipartícula resultante de la cuantificación de las oscilaciones del plasma. Así, los plasmones son oscilaciones colectivas de la densidad de gas de electrones libres, a menudo a frecuencias ópticas. Pueden acoplarse a un fotón para crear una tercera cuasipartícula llamada polaritón de plasma.
En los plasmones superficiales, en lugar de tener oscilaciones colectivas de un gas, tenemos una oscilación colectiva de los electrones de conducción de un metal. Más precisamente, los plasmones superficiales son plasmones confinados a superficies que interactúan fuertemente con la luz, resultando en un polaritón plasmónico superficial (o onda plasmónica superficial).
La imagen de la celda de flujo recuperada por el software corresponde a la imagen en tiempo real de la superficie SPRi-Biochip. La imagen de diferencia muestra puntos interactuantes cuando se inyecta la solución de analito.
La imagen permite monitorizar simultáneamente las condiciones de resonancia en la superficie del SPRi-Biochip. Si el SPRi-Biochip contiene diferentes moléculas inmovilizadas (formato de array), las interacciones potenciales sobre esas moléculas distintas (también llamadas ligandos o puntos) se monitorizan en paralelo, gracias al uso de una cámara. Esta propiedad (medición simultánea de todos los elementos del microarray) también se denomina a menudo multiplexación. La función de imagen de nuestros dispositivos permite la medición multiplex de hasta varios cientos de interacciones.
La imagen de la celda de flujo recuperada por el software corresponde a la imagen en tiempo real de la superficie SPRi-Biochip. La imagen de diferencia muestra puntos interactuantes cuando se inyecta la solución de analito.
Curva de interacción cinética: (A) tiempo de latencia, (B) asociación, (C) saturación, (D) disociación, (E) regeneración.
Cuando se inyecta la solución muestra, el analito debe alcanzar la celda de flujo para interactuar con el ligando. Este periodo de tiempo en el que el analito aún no está en la celda de flujo se denomina tiempo de latencia (A).
Luego se inyecta la muestra, los analitos atraviesan la celda de flujo e interactúan con los ligandos en la superficie. Este paso se denomina fase de asociación (B). Se alcanza una meseta (C) al final de la asociación y esto puede explicarse por estados moleculares (equilibrio, saturación o volumen inyectado terminado). Cuando ya no pasan más analitos por la celda de flujo, la solución de analitos es reemplazada por el buffer en marcha, y los analitos se disocian de los ligandos inmovilizados, es la fase de disociación (D).
Algunas interacciones tienen una alta afinidad y algunos analitos pueden seguir uniéndose a los ligandos tras el paso de disociación. En este caso, se inyecta una solución de regeneración para eliminar todos los analitos restantes. Este es el paso de regeneración (E). A continuación, se puede inyectar una nueva solución de muestra.
Parámetros cinéticos
k un es la constante de tasa de asociación (M-1.s-1), en algunos casos, también se le llama k culo k d es la constante de tasa de disociación (s-1), en algunos casos, también se le llama k Diss.
Los datos de cinética SPR (interacciones) pueden modelarse simplemente para evaluar la afinidad entre 2 moléculas. El modelo generalmente utilizado asume que las reacciones involucran un ligando (L) y un analito (A) que interactúan con una estequiometría 1:1:
![]()
Este modelo ofrece las siguientes fórmulas para nuestras curvas cinéticas de interacción, una para la respuesta de asociación (R a) y otra para la respuesta de disociación (R d), siendo en nuestro caso la variación de reflectividad:
R a (t)= R eq •(1-exp[-k obs •(t-t 0)]) (asociación)
R d (t)=R d(t 1) • exp[-k off •(t-t 1)] (disociación)
con k obs = k ass • C i +k diss, la constante observada de la respuesta durante la asociación, C i la concentración de analito inyectado y k off = k diss, la constante de velocidad de desconexión de la respuesta durante la disociación, t 0 y t 1 indican respectivamente el inicio de la asociación y de la disociación.
En resumen, los parámetros cinéticos k ass y k diss se calculan ajustando cada parte de la interacción (asociación y disociación) con una curva monoexponencial, preferentemente usando el software ScrubberGen o EzFit (basado en Scrubber).
Parámetros de afinidad
K A es la constante de afinidad (M-1)
K D es la constante de equilibrio (M)
Conociendo los parámetros cinéticos, se puede deducir la constante de afinidad entre 2 moléculas:
K A = 1/K D = K A / K D
Los parámetros de afinidad también pueden calcularse a partir de valores de equilibrio con un ajuste de Langmuir.
Parámetros termodinámicos
ΔG es el cambio de energía libre
ΔH es el cambio de entalpía
ΔS es el cambio de entropía
Se puede calcular a partir de la constante de afinidad (o de la constante de disociación):
ΔG = R • T • ln(K D)
donde R es la constante de gas, T es la temperatura absoluta (K) y KD se expresa en M.
Para calcular ΔH y ΔS, los parámetros de afinidad deben determinarse a varias temperaturas. ΔG se deduce de estos valores en un rango de temperaturas. La ecuación no lineal de Van't Hoff se ajusta a los datos para determinar ΔH, ΔS:
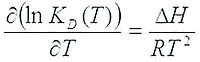
Luego, sabiendo que ΔG = ΔH-T•ΔS, también se puede evaluar el cambio de entropía.